
本文由April Chen原創,發表在“新浪醫(yī)藥”公衆号上(shàng)
目前全世界有超過2600萬人(rén)患有心衰,在中國(guó),心衰的患病率為(wèi)0.9%,估計有400-500萬心衰患者。随着年(nián)齡的增高,生活習慣改變肥胖和(hé)2型糖尿病患者人(rén)群增多等,心衰的患病率顯著上(shàng)升。
導緻心衰的原因很(hěn)多,但(dàn)臨床表現都(dōu)是心髒輸出率降低(dī)。根據左心室射血分數(shù)(LVEF)降低(dī)程度,分為(wèi)射血分數(shù)降低(dī)(LVEF<40%)的心衰(HFrEF)、射血分數(shù)中間(jiān)值(LVEF 40–49%)的心衰(HFmrEF)和(hé)射血分數(shù)保留(LVEF >49%)的心衰(HFpEF),其中HFrEF約一(yī)半,盡管目前有多種治療藥物(wù),但(dàn)是5年(nián)死亡率高達75%。而對于其餘兩類心衰,目前尚無藥物(wù)批準,通(tōng)常僅能(néng)減輕症狀和(hé)超說明(míng)書(shū)使用治療HFrEF藥物(wù)。
心衰藥物(wù)市場多年(nián)來都(dōu)是被仿制藥占據,主要(yào)為(wèi)利尿劑,ACE抑制劑和(hé)ARB抑制劑等,慢(màn)病管理成本壓力和(hé)臨床試驗投入巨大,心衰新藥開(kāi)發市場具有挑戰性,目前開(kāi)發策略都(dōu)是與标準療法聯用。
Entresto起步較晚,已成為(wèi)心衰重磅炸彈藥物(wù)
諾華Entresto (sacubitril腦啡肽酶抑制劑/缬沙坦) 于2015年(nián)7月和(hé)11月先後在美國(guó)和(hé)歐盟獲批,用于治療HFrEF成人(rén)患者。Entresto是首個與ACE抑制劑依那(nà)普利比較的頭對頭試驗中顯示出顯著生存獲益的治療藥物(wù),死亡率降低(dī)20%。
諾華上(shàng)一(yī)代心血管産品線重磅炸彈藥物(wù)就是大名鼎鼎的Diovan(缬沙坦),Entresto作(zuò)為(wèi)其延續和(hé)擴充一(yī)直被看(kàn)好,但(dàn)初期市場表現因價格和(hé)醫(yī)保問(wèn)題而銷售低(dī)于預期,在進入多數(shù)保險公司醫(yī)保目錄後,患者仍要(yào)自(zì)付一(yī)千多美金(jīn)的藥費(fèi)。随着Entresto獲得歐美各大指南I類推薦,2018年(nián)銷售終于突破10億美元。目前美國(guó)本土(tǔ)和(hé)其他(tā)地(dì)區(qū)銷售量各占一(yī)半,是諾華增長(cháng)率第二的産品,2019年(nián)12月通(tōng)過中國(guó)醫(yī)保談判納入醫(yī)保乙類,2020年(nián)即将在日本上(shàng)市,銷量還會繼續增長(cháng)。
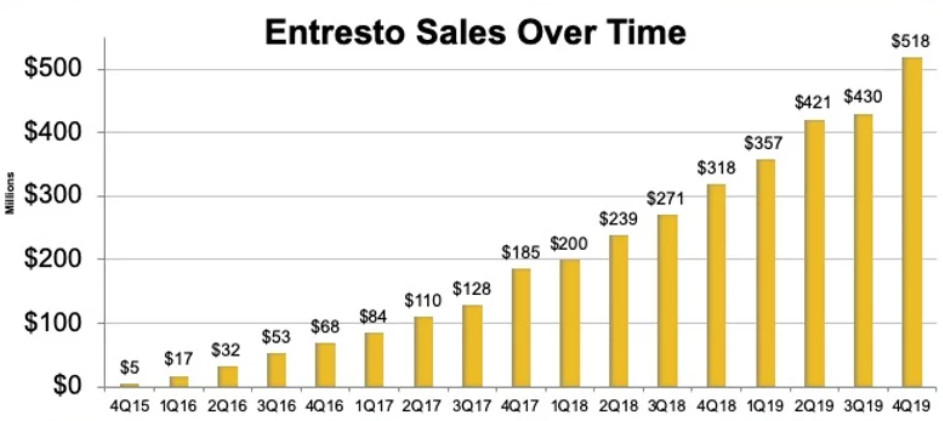
圖1 Entresto全球銷量(百萬美元)
想要(yào)在心衰市場做(zuò)出差異化,Entresto需要(yào)擴展至目前沒有藥物(wù)批準的HFpEF患者人(rén)群。與HFrEF相比,HFpEF症狀較輕、死亡率較低(dī),這(zhè)使得目前藥物(wù)開(kāi)發難以證明(míng)其獲益。
2019年(nián)7月,評估Entresto對比缬沙坦治療HFpEF的全球性III期臨床研究PARAGON-HF的試驗沒有達到主要(yào)終點——降低(dī)心衰住院和(hé)心血管死亡,共入組了(le)4822例患者,從(cóng)多個次要(yào)終點結果看(kàn),Entresto在某些特定人(rén)群中有一(yī)定優勢,例如(rú)Entresto與缬沙坦組腎功能(néng)惡化程度比例分别為(wèi)1.4%和(hé)2.7%(HR=0.5),還有在女(nǚ)性和(hé)HF-mrEF的患者人(rén)群中顯示獲益,Entresto也許可(kě)以嘗試在這(zhè)些亞組人(rén)群中繼續探索。
除此之外(wài),2019年(nián)諾華還公布了(le)Entresto另外(wài)兩個試驗結果,在PROVE-HF試驗中Entresto證明(míng)能(néng)降低(dī)NT-proBNP水平,和(hé)改善心髒結構;在EVALUATE-HF試驗中,Entresto或者依那(nà)普利均未改善主要(yào)終點即主動脈阻抗(血管硬度的測量指标)變化,但(dàn)Entresto在左心室的結構和(hé)功能(néng)上(shàng)顯示出積極的結果,這(zhè)意味着它可(kě)以逆轉由射血分數(shù)(HF-REF)降低(dī)的心力衰竭所緻的心髒損傷。
Entresto幾乎是諾華在心衰産品線重金(jīn)開(kāi)發的産品,除了(le)HFpEF外(wài),目前還在進行(xíng)用于兒童心衰、急性心肌梗塞後心衰等III期臨床試驗。
另一(yī)個心衰候選藥物(wù)CLR325在2020年(nián)不作(zuò)為(wèi)心血管研發管線的主要(yào)開(kāi)發藥物(wù)。
SGLT2抑制劑強勢進入心衰治療市場
阿斯利康的SGLT2抑制劑Farxiga(達格列淨)在2019年(nián)10月獲得FDA批準,用于降低(dī)存在心血管疾病(CVD)或多個心血管(CV)風(fēng)險因素的2型糖尿病成人(rén)患者的心衰住院或CV死亡風(fēng)險,相比安慰劑降低(dī)風(fēng)險17%。
目前在心衰适應症抓住了(le)機遇,2020年(nián)1月,Farxiga(達格列淨)用于降低(dī)伴或不伴2型糖尿病、HFrEF成人(rén)患者降低(dī)心衰惡化或CV死亡風(fēng)險的上(shàng)市申請(qǐng),獲得FDA優先審查。基于名為(wèi)DAPA-HF的III期試驗,納入的4744位伴有或不伴有2型糖尿病的HFrEF患者,與标準療法聯用,Farxiga比安慰劑顯著降低(dī)心血管(CV)死亡或心衰惡化複合終點的風(fēng)險26%(p<0.0001)。
2019年(nián)6月,FDA授予Jardiance(恩格列淨)用于降低(dī)HFrEF患者的心衰住院或CV死亡風(fēng)險快(kuài)速通(tōng)道(dào)資格,主要(yào)基于正在進行(xíng)的EMPEROR項目,包括EMPEROR-Reduced和(hé)EMPEROR-Preserved,分别用于HFrEF和(hé)HFpEF患者的III期研究,試驗結果計劃于2020年(nián)完成試驗。但(dàn)在2019年(nián)12月公布的兩個名為(wèi)EMPERIAL-reduced和(hé)EMPERIAL-preserved的III期試驗未達到主要(yào)終點指标,與安慰劑相比,恩格列淨未能(néng)改善心衰患者運動功能(néng)(以6分鐘(zhōng)走路距離評估)。
達格列淨有可(kě)能(néng)是首個批準用于HFrEF的SGLT-2抑制劑,恩格列淨雖然在心衰患者運動功能(néng)試驗中失敗,目前在同時(shí)進行(xíng)用于HFrEF和(hé)HFpEF兩個人(rén)群的EMPEROR試驗結果,結果都(dōu)将在今年(nián)揭曉。SGLT-2抑制劑在糖尿病适應症無法超越DPP-4抑制劑銷量,但(dàn)心衰大病種若獲批,銷售量有望迎來又一(yī)輪攀升。
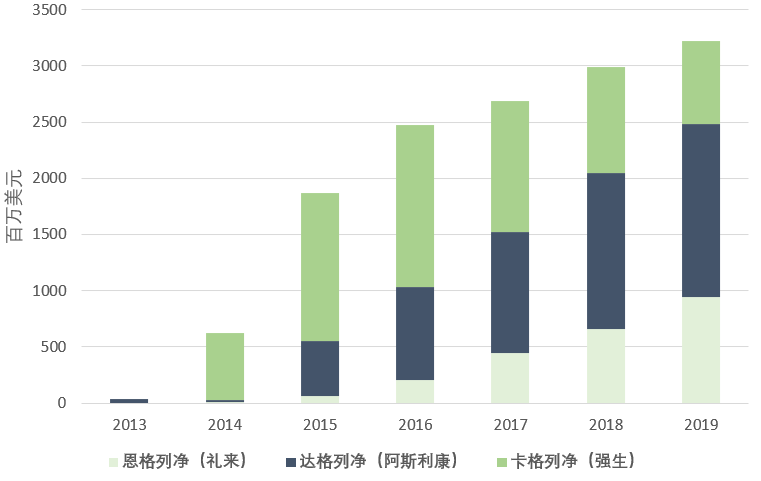
圖2 三大SGLT-2抑制劑全球銷售額
全新機制新藥中,Vericiguat有望2020年(nián)遞交上(shàng)市申請(qǐng)
在臨床III期階段,還有3個全新作(zuò)用機制的新藥Vericiguat、omecamtiv mecarbil和(hé)重組紐蘭格林。
拜耳一(yī)直是心血管市場的引領者,在肺動脈高壓、血栓症、高血壓、心衰等領域都(dōu)有産品和(hé)研發管線布局。2019年(nián)11月,拜耳與默克共同開(kāi)發的vericiguat,3期臨床研究VICTORIA達到了(le)主要(yào)終點,納入了(le)5,050例HFrEF患者,與安慰劑相比,可(kě)以降低(dī)這(zhè)些患者的心力衰竭住院或心血管死亡的複合終點風(fēng)險。Vericiguat是首個開(kāi)發用于治療慢(màn)性心力衰竭惡化患者的“first-in-class”可(kě)溶性鳥苷酸環化酶(sGC)激動劑,sGC功能(néng)低(dī)下(xià)導緻cGMP水平不足與心機損傷有關,同時(shí),sGC作(zuò)為(wèi)NO的受體之一(yī),能(néng)提高NO-sGC-cGMP通(tōng)路的活性。
盡管在IIb期用于HFpEF人(rén)群的試驗SOCRATES-Preserved失敗了(le),10mg的vericiguat與安慰劑比較,未能(néng)顯著提高主要(yào)終點指标心衰标記物(wù)腦鈉肽前體(NT-proBNP),但(dàn)事後分析發現能(néng)顯著提高生活質量量表,于是拜耳和(hé)默克還是決定繼續向HFpEF人(rén)群推進,開(kāi)啓了(le)名為(wèi)Vitality-HFpEF的II期試驗。
手握PCSK9抑制劑Repatha的安進也是心血管疾病領域的主要(yào)玩(wán)家,在心衰藥物(wù)開(kāi)發人(rén)群則選擇另辟蹊徑,處于臨床III期的omecamtiv mecarbil是一(yī)種心肌肌球蛋白激活劑,與安進在2015年(nián)上(shàng)市的伊伐布雷定類似,都(dōu)選擇開(kāi)發人(rén)群較小的,LVEF≤35%,具有心血管事件高風(fēng)險的HFrEF患者。
與之前提及的擁有成熟心血管産品管線的大公司不同,重組紐蘭格林是澤生生物(wù)進入臨床開(kāi)發的唯一(yī)藥物(wù),這(zhè)是一(yī)種來源于人(rén)體內(nèi)自(zì)然存在的Neuregulin-1的活性多肽片段,屬于重組蛋白藥物(wù),通(tōng)過結合受損心肌細胞表面的ErbB4受體,以達到修複心肌細胞結構、改善心髒舒張功能(néng)的作(zuò)用。2020年(nián)2月12日在中國(guó)的上(shàng)市申請(qǐng)未被獲批,審評意見(jiàn)中指出,除了(le)繼續目前正在進行(xíng)的HFrEF患者以全因死亡率為(wèi)主要(yào)終點的III期臨床試驗,還需要(yào)補充一(yī)個以心功能(néng)(LVEF、患者心衰症狀)為(wèi)主要(yào)療效指标,以終點事件為(wèi)次要(yào)療效指标/安全性指标的III期臨床試驗。如(rú)果能(néng)夠重現既往臨床研究中觀察到的心功能(néng)獲益結果,可(kě)考慮申請(qǐng)有條件批準上(shàng)市。
在2019年(nián)6月,FDA發布了(le)《心力衰竭的治療:藥物(wù)臨床試驗的試驗終點行(xíng)業指南(征求意見(jiàn)稿)》中指出,如(rú)果一(yī)個心衰新藥即使不能(néng)改善生存或住院率,若在症狀或功能(néng)方面提供了(le)有實質性和(hé)持續性的改善,特别是對于紐約心髒病協會III級或IV級心衰患者,是可(kě)以被FDA批準的;生存率可(kě)以作(zuò)為(wèi)一(yī)個心衰新藥臨床試驗主要(yào)終點,或安全性終點。
表1 部分臨床階段用于心衰開(kāi)發的藥物(wù)
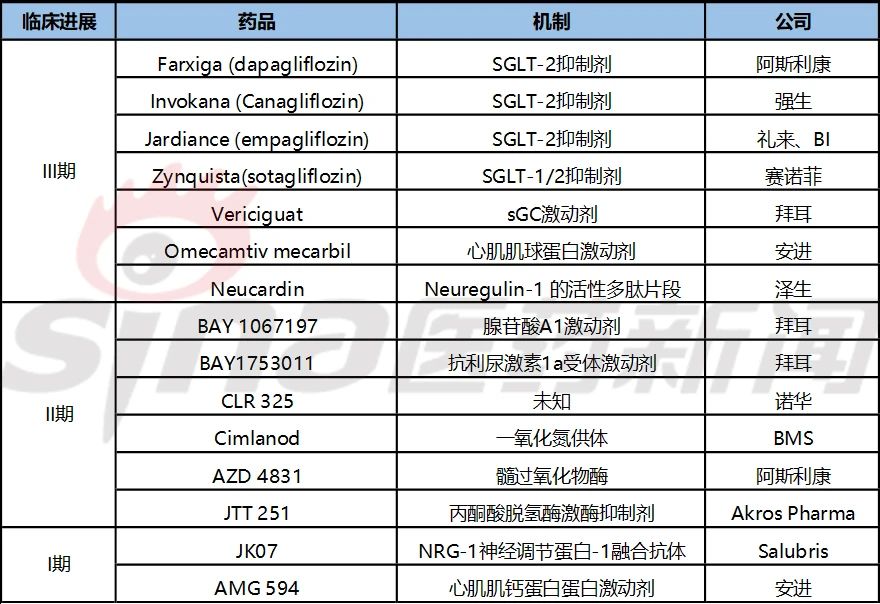
參考資料:
1、Vaduganathan M, Claggett B, Desai A, et al. Prior Heart Failure Hospitalization, Clinical Outcomes, and Response to Sacubitril/Valsartan Compared with Valsartan in HFpEF. JACC 2019. doi: 10.1016/j.jacc.2019.11.003.
2、phase III randomised, double-blind trial to evaluate the effect of 12 weeks treatment of once daily EMPagliflozin 10 mg compared with placebo on ExeRcise ability and heart failure symptoms, In patients with chronic HeArt FaiLure with preserved Ejection Fraction (HFpEF) (EMPERIAL – preserved). Available at: https://clinicaltrials.gov/ct2/show/NCT03448406?term=EMPERIAL&rank=1. Last accessed February 2018.
3、A phase III randomised, double-blind trial to evaluate the effect of 12 weeks treatment of once daily EMPagliflozin 10 mg compared with placebo on ExeRcise ability and heart failure symptoms, In patients with chronic HeArt FaiLure with reduced Ejection Fraction (HFrEF) (EMPERIAL – reduced). Available at: https://clinicaltrials.gov/ct2/show/NCT03448419?term=EMPERIAL&rank=2. Last accessed February 2018.
4、https://www.fda.gov/regulatory-information/search-fda-guidance-documents/treatment-heart-failure-endpoints-drug-development-guidance-industry
5、各大公司官網
6、Pharmadigger數(shù)據庫