
本文選自(zì):中國(guó)臨床藥理學雜(zá)志 第39卷 第7期1060-1064
作(zuò)者簡介:劉美霞,主管藥師(shī),主要(yào)從(cóng)事藥物(wù)技術(shù)審評工(gōng)作(zuò)
通(tōng)信作(zuò)者:王駿,研究員(yuán)
作(zuò)者單位:國(guó)家藥品監督管理局 藥品審評中心
化學藥品改良型新藥是在已知活性成分的基礎上(shàng),對其結構、劑型、處方工(gōng)藝、給藥途徑、适應證等進行(xíng)優化,具有明(míng)顯臨床優勢的藥品。不同于全新靶點和(hé)結構創新藥研發的高投入、長(cháng)周期、高風(fēng)險,改良型新藥可(kě)借鑒已知活性成分藥品的研究數(shù)據,降低(dī)研發成本、縮短臨床研發的周期、提高臨床成功率。随着制藥工(gōng)業技術(shù)的快(kuài)速發展,改良型新藥已成為(wèi)當前新藥研發的熱(rè)點方向之一(yī)。改良型新藥的評價通(tōng)常基于整體證據,包括藥學、非臨床及臨床研究內(nèi)容。其中,臨床藥理研究對改良型新藥的開(kāi)發至關重要(yào)。目前,國(guó)內(nèi)已發布《化學藥品改良型新藥臨床試驗技術(shù)指導原則》和(hé)《改良型新藥調釋制劑臨床藥代動力學研究技術(shù)指導原則》,尚未發布針對改良型新藥臨床藥理研究的指導原則。國(guó)內(nèi)已申報的化學藥品改良型新藥中,臨床藥理研究主要(yào)存在以下(xià)問(wèn)題:①對于簡單的不改變藥代動力學(PK)特征的改劑型類改良型新藥,試驗過程中未驗證臨床優勢,如(rú)口崩片的臨床優勢為(wèi)在口腔中直接崩解後服用,無需用水送服,但(dàn)實際試驗過程中此類制劑往往未進行(xíng)無水服藥的相對生物(wù)利用度研究。②對于改變PK特征的改良型新藥,在臨床試驗過程中,經常存在改良型新藥與對照制劑的PK特征比對不充分,劑量探索研究缺失,食物(wù)效應、藥物(wù)相互作(zuò)用研究等外(wài)因對藥物(wù)體內(nèi)暴露影響的研究欠缺等問(wèn)題,從(cóng)而導緻無法為(wèi)改良型新藥的臨床用法用量提供充分的科學依據。本文主要(yào)結合美國(guó)食品藥品監督管理局(FDA)已上(shàng)市化學藥品改良型新藥研究實例及審評過程中遇到的問(wèn)題,對化學藥品改良型新藥的臨床藥理研究提出幾點思考,以期為(wèi)國(guó)內(nèi)化學藥品改良型新藥的研發提供一(yī)些參考。
1 昂丹司瓊口溶膜
昂丹司瓊原研企業為(wèi)葛蘭素史克,片劑(商品名:Zofran)于1992年(nián)獲FDA批準上(shàng)市,口崩片(商品名:Zofran ODT)于1999年(nián)獲FDA批準上(shàng)市。昂丹司瓊臨床上(shàng)主要(yào)作(zuò)為(wèi)止吐藥,用于由細胞毒性藥物(wù)化療和(hé)放射治療引起的惡心嘔吐,也可(kě)用于預防和(hé)治療手術(shù)後的惡心嘔吐。為(wèi)了(le)提高吞咽困難患者的順應性,Par Pharmaceuticals, Inc.開(kāi)發了(le)昂丹司瓊口溶膜(商品名:Zuplenz),并于2010年(nián)通(tōng)過505b(2)途徑在FDA獲批上(shàng)市。昂丹司瓊口溶膜上(shàng)市時(shí)開(kāi)展的臨床研究,見(jiàn)表1。
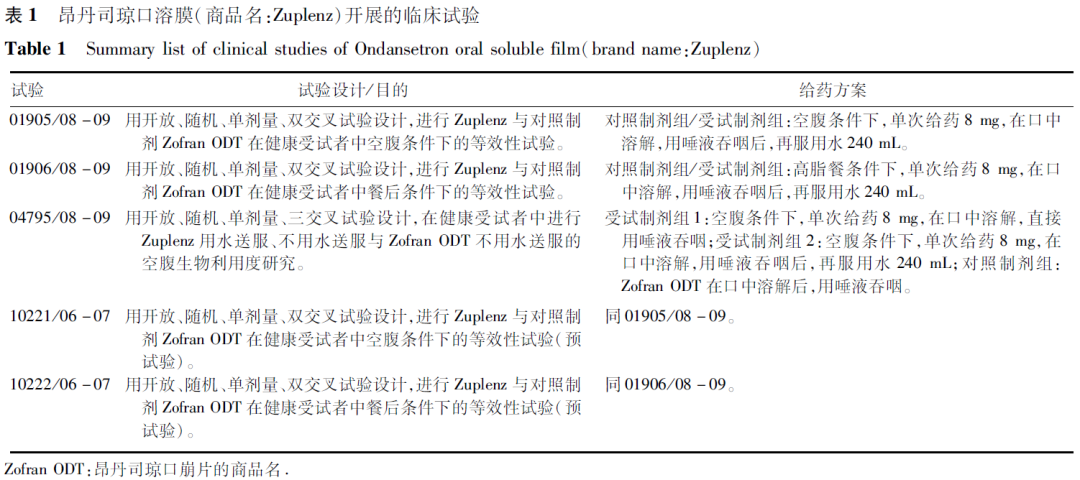
昂丹司瓊口溶膜上(shàng)市時(shí)主要(yào)通(tōng)過空腹、餐後2項關鍵性生物(wù)等效性試驗橋接原研昂丹司瓊口崩片的安全有效性數(shù)據(含成人(rén)及兒科患者人(rén)群):昂丹司瓊口溶膜與昂丹司瓊口崩片在空腹、高脂餐後條件下(xià),單次口服8 mg具有生物(wù)等效性,昂丹司瓊口溶膜在舌頭上(shàng)溶解時(shí)間(jiān)稍長(cháng)于昂丹司瓊口崩片,約快(kuài)3~4
s。同時(shí)考察了(le)昂丹司瓊口溶膜不同服藥方式對相對生物(wù)利用度的影響:在健康受試者空腹條件下(xià),用水送服、無需水送服昂丹司瓊片8 mg與無需水送服昂丹司瓊口崩片8 mg具有生物(wù)等效性。
2 醋酸阿比特龍片
原研Janssen
Biotech的醋酸阿比特龍片(商品名:ZYTIGA)于2011年(nián)4月在美國(guó)獲批上(shàng)市,2015年(nián)獲批進口國(guó)內(nèi)。醋酸阿比特龍片在臨床上(shàng)主要(yào)與潑尼松或潑尼松龍合用,用于前列腺癌的治療。醋酸阿比特龍片的推薦劑量為(wèi)每日1 000 mg,單次服用;至少(shǎo)在服藥前2 h內(nèi)和(hé)服藥後1 h內(nèi)不能(néng)進食。醋酸阿比特龍片存在生物(wù)利用度低(dī)、體內(nèi)暴露個體變異大且食物(wù)影響顯著等問(wèn)題。
Sun
Pharma Global, FZE的醋酸阿比特龍改良型新藥于2018年(nián)5月通(tōng)過505b(2)途徑在FDA獲批上(shàng)市,商品名為(wèi)YONSA,用SoluMatrix微(wēi)粒技術(shù)制造工(gōng)藝,提供了(le)一(yī)種微(wēi)粒化的醋酸阿比特龍片劑,使其在體內(nèi)能(néng)被更有效地(dì)吸收,從(cóng)而減少(shǎo)了(le)臨床使用劑量,降低(dī)了(le)食物(wù)因素的影響。醋酸阿比特龍片(商品名:YONSA)推薦劑量為(wèi)500 mg,每日1次,空腹或餐後口服。申報上(shàng)市時(shí)開(kāi)展的臨床試驗見(jiàn)表2,包括4項PK研究和(hé)1項基于睾酮抑制的PK/藥效學(PD)研究。
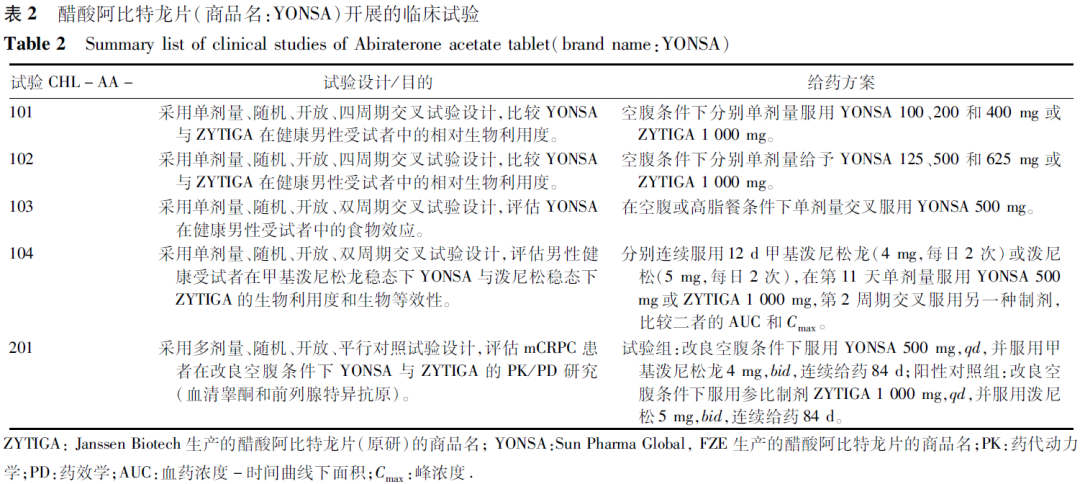
臨床藥理研究結果顯示:阿比特龍在125~625
mg內(nèi),AUC呈劑量比例增加,Cmax呈略微(wēi)低(dī)劑量比例增加。醋酸阿比特龍片(商品名:YONSA)與醋酸阿比特龍片(商品名:ZYTIGA)兩制劑PK方面的差異主要(yào)在吸收和(hé)生物(wù)利用度方面。健康男(nán)性受試者單次給藥醋酸阿比特龍片(商品名:YONSA) 500 mg與單次給藥醋酸阿比特龍片(商品名:ZYTIGA)1 000 mg具有生物(wù)等效性。健康受試者空腹或高脂餐後單劑量服用醋酸阿比特龍片(商品名:YONSA) 500 mg,高脂餐後阿比特龍的Cmax和(hé)AUCinf是隔夜空腹條件下(xià)的6.5倍和(hé)4.4倍。穩态甲潑尼松龍/潑尼松下(xià),空腹條件下(xià)單次給藥醋酸阿比特龍片(商品名:YONSA) 500 mg與空腹單次給藥醋酸阿比特龍片(商品名:ZYTIGA) 1 000 mg阿比特龍在人(rén)體內(nèi)的系統暴露量相似。轉移性去勢抵抗性前列腺癌(mCRPC)患者在改良空腹條件下(xià)多次給藥後的主要(yào)有效性終點——第9和(hé)10天平均血清睾酮水平,醋酸阿比特龍片(商品名:YONSA;n=24)和(hé)醋酸阿比特龍片(商品名:ZYTIGA;n=28)睾酮抑制情況相似;醋酸阿比特龍片(商品名:YONSA)在改良空腹條件下(xià)多次給藥後的穩态暴露量低(dī)于醋酸阿比特龍片(商品名:ZYTIGA)。最終醋酸阿比特龍片(商品名:YONSA)基于與醋酸阿比特龍片(商品名:ZYTIGA)的PK、PD相似性在FDA獲批上(shàng)市。
綜上(shàng),醋酸阿比特龍改良型新藥目的為(wèi)避免食物(wù)影響,增加生物(wù)利用度,降低(dī)服用劑量。在探索到目标制劑與對照制劑臨床用藥暴露量相當的劑量後,進行(xíng)該劑量下(xià)本品相應用法下(xià)的最低(dī)和(hé)最高暴露量研究,并與對照制劑醋酸阿比特龍片(商品名:ZYTIGA)進行(xíng)對比。醋酸阿比特龍片(商品名:YONSA)的暴露量上(shàng)下(xià)限分别不超過後者暴露量的上(shàng)下(xià)限或達到生物(wù)等效。
3 伊立替康脂質體注射液
伊立替康在人(rén)體組織內(nèi)由非特異性羧酸酯酶轉化為(wèi)活性代謝(xiè)物(wù)SN-38發揮主要(yào)治療作(zuò)用。SN-38通(tōng)過關鍵代謝(xiè)酶——尿苷二磷酸葡糖醛酸轉移酶1A1(UGT1A1)轉換為(wèi)SN-38G(使用2種細胞系的體外(wài)細胞毒性測定中SN-38G的活性為(wèi)SN-38的1/50至1/100)經膽汁及尿液排出。UGT1A1具有基因多态性,可(kě)導緻SN-38葡糖醛酸化速率産生50倍差異。
普通(tōng)鹽酸伊立替康注射液及其凍幹粉針制劑在體內(nèi)易被代謝(xiè)失活,采用脂質體劑型可(kě)以合理地(dì)改善伊立替康的PK和(hé)生物(wù)分布,同時(shí)保護其免于過早代謝(xiè)。
Merrimack
Pharmaceuticals公司開(kāi)發的伊立替康脂質體注射液(商品名:Onivyde;MM-398)于2015年(nián)通(tōng)過505b(2)途徑在FDA獲批上(shàng)市。伊立替康脂質體注射液在FDA申報上(shàng)市時(shí),開(kāi)展的臨床試驗見(jiàn)表3,共包括6項與臨床藥理相關的研究及1項群體PK研究。

以上(shàng)研究結果表明(míng):伊立替康脂質體的直接測定表明(míng),95%的伊立替康在循環過程中仍保持脂質體包封。與伊立替康注射劑(商品名:Camptosar)相比,輸注MM-398後,總伊立替康的暴露量更高,SN-38的t1/2(3.0倍)和(hé)AUC0-inf(1.4倍)更高,但(dàn)Cmax降低(dī)(0.19倍)。輸注伊立替康脂質體注射液(商品名:Onivyde)、伊立替康注射劑(商品名:Camptosar)後,伊立替康轉化為(wèi)SN-38的轉化率分别為(wèi)2.89×10-4和(hé)1.50×10-2,SN-38轉化為(wèi)SN-38G的轉化率分别為(wèi)11.5和(hé)16.4,大部分的伊立替康以脂質體形式存在,限制了(le)MM-398轉化為(wèi)SN-38。
群體PK研究結果表明(míng):年(nián)齡、性别對伊立替康和(hé)SN-38的暴露沒有臨床意義的影響;在調整了(le)體表面積(BSA)後,輕度到中度腎損害對總SN-38的暴露沒有影響。基線總膽紅(hóng)素濃度為(wèi)1~2 mg·dL-1(n=19)的患者總SN-38的平均穩态濃度比基線膽紅(hóng)素濃度<1 mg·dL-1(n=329)的患者增加了(le)37%;對UGT1A1*28純合子患者給予較低(dī)劑量伊立替康脂質體,該等位基因的純合子(n=14)和(hé)非純合子(n=244)患者的總SN-38平均穩态濃度分别為(wèi)1.06和(hé)0.95 ng·mL-1;亞洲人(rén)總伊立替康平均穩态濃度比高加索人(rén)低(dī)56%,總SN-38平均穩态濃度高8%。
劑量-暴露-效應關系分析結果顯示:在證明(míng)本品有效性的臨床試驗中,伊立替康脂質體+5-FU/LV治療組患者的總伊立替康和(hé)SN-38血漿暴露水平升高與總生存期(OS)和(hé)無進展生存期(PFS)較長(cháng)以及客觀緩解率(ORR)較高相關。在353例患者的彙總分析中,血漿SN-38 Cmax較高與出現中性粒細胞減少(shǎo)症的可(kě)能(néng)性增加有關,血漿總伊立替康Cmax較高與出現腹瀉可(kě)能(néng)性增加有關。
綜上(shàng),伊立替康脂質體注射液通(tōng)過采用脂質體劑型改善伊立替康的PK和(hé)生物(wù)分布,保護其免于過早代謝(xiè)。伊立替康脂質體注射液的臨床藥理研究主要(yào)通(tōng)過在患者中的單藥劑量遞增研究、聯合用藥的劑量遞增研究獲得本品的最大耐受劑量及初步PK特征;通(tōng)過與普通(tōng)制劑的比對研究進一(yī)步确認本品與普通(tōng)制劑相比的PK行(xíng)為(wèi)差異;通(tōng)過群體PK研究與暴露-效應關系分析為(wèi)特殊人(rén)群(含基因多态性)給藥劑量調整提供依據。
4 讨
論
結合FDA獲批上(shàng)市的昂丹司瓊口溶膜、醋酸阿比特龍片、伊立替康脂質體注射液改良型新藥的臨床藥理研究情況及同類品種國(guó)內(nèi)申報情況,對化學藥品改良型新藥的臨床藥理研究提出以下(xià)幾點思考。
對于普通(tōng)的改劑型藥物(wù),如(rú)片劑、膠囊劑、分散片、顆粒劑、幹混懸劑、口溶膜、無水吞服顆粒等普通(tōng)口服劑型之間(jiān)的劑型改變,通(tōng)常不會改變藥物(wù)的PK特征。對該類改良型新的臨床藥理研發思路,通(tōng)常可(kě)通(tōng)過與對照制劑進行(xíng)相對生物(wù)利用度/生物(wù)等效性研究,橋接對照制劑的安全有效性數(shù)據。改良型新藥與對照制劑的相對生物(wù)利用度/生物(wù)等效性研究同普通(tōng)仿制藥的生物(wù)等效性研究不同,研究過程中需驗證目标制劑的臨床優勢,例如(rú)對于普通(tōng)片改為(wèi)口溶膜的改良型新藥,口溶膜可(kě)在口腔內(nèi)溶解後直接吞咽,提高吞咽困難患者的順應性,在進行(xíng)相對生物(wù)利用度/生物(wù)等效性研究的過程中,需考察口溶膜無水吞服給藥方式下(xià)的相對生物(wù)利用度以及在口腔內(nèi)的溶解時(shí)間(jiān)等。通(tōng)過優化制劑處方工(gōng)藝等改變生物(wù)利用度的藥物(wù),如(rú)普通(tōng)口服制劑改為(wèi)調釋口服制劑,普通(tōng)靜脈注射劑改為(wèi)皮下(xià)給藥注射劑等,該類改良型新藥的臨床藥理研發思路,通(tōng)常基于活性成分達到與對照制劑相似的暴露量,從(cóng)而橋接對照制劑的安全有效性數(shù)據。在探索到目标制劑與對照制劑臨床用藥暴露量相當的劑量後,進一(yī)步考察外(wài)因如(rú)食物(wù)效應等因素對體內(nèi)暴露行(xíng)為(wèi)的影響,為(wèi)臨床用法用量提供科學依據。
對于食物(wù)效應研究,通(tōng)常建議(yì)頭對頭比較目标制劑在空腹、高脂餐條件下(xià)的體內(nèi)暴露量與對照制劑獲批的空腹和(hé)/或高脂餐條件下(xià)的體內(nèi)暴露量差異,推薦采用三交叉或四交叉研究設計。對需要(yào)聯合用藥的藥物(wù),為(wèi)考察聯合用藥對目标制劑與對照制劑的系統暴露量的影響,通(tōng)常需開(kāi)展聯合用藥後的相對生物(wù)利用度/生物(wù)等效性研究。
對于改變藥物(wù)吸收及組織分布的改良型新藥,如(rú)普通(tōng)注射劑改為(wèi)脂質體、微(wēi)球等,通(tōng)過改變活性藥物(wù)的釋放特征以及在機體的吸收、組織分布,導緻藥物(wù)在體內(nèi)PK特征發生明(míng)顯改變。對該類藥物(wù)一(yī)般無法通(tōng)過體內(nèi)暴露量直接橋接對照制劑的安全、有效性數(shù)據,臨床藥理研究主要(yào)為(wèi)探索目标藥物(wù)的PK特征和(hé)劑量-暴露-效應關系,确立給藥方案。進行(xíng)該類藥物(wù)與對照制劑的PK比對研究,闡述二者在吸收、分布、代謝(xiè)和(hé)排洩方面的差異,有利于尋找最佳臨床給藥方案。此類藥物(wù)可(kě)參照《化學藥創新藥臨床單次和(hé)多次給藥劑量遞增PK研究技術(shù)指導原則》《創新藥臨床藥理學研究技術(shù)指導原則》等進行(xíng)相關研究。
需要(yào)說明(míng)的是,本文是基于目前的科學認知、背景調研等提出的化學藥品改良型新藥臨床藥理研究的相關考慮,不代表監管機構的要(yào)求。