
本文為(wèi)找藥寶典公衆号原創文章(zhāng)
前言
近期,肺癌靶向治療進展非常迅速,無論是國(guó)內(nèi)或國(guó)外(wài),有不少(shǎo)高效的靶向藥接連提交上(shàng)市申請(qǐng),并且有些藥也以光(guāng)速獲批上(shàng)市。随着新藥猛進,肺癌靶向治療又迎來了(le)新一(yī)波的巅峰,藥物(wù)靶點涵蓋EGFR,ALK,MET,KRAS,RET,一(yī)起來看(kàn)看(kàn)這(zhè)些新型藥物(wù)。
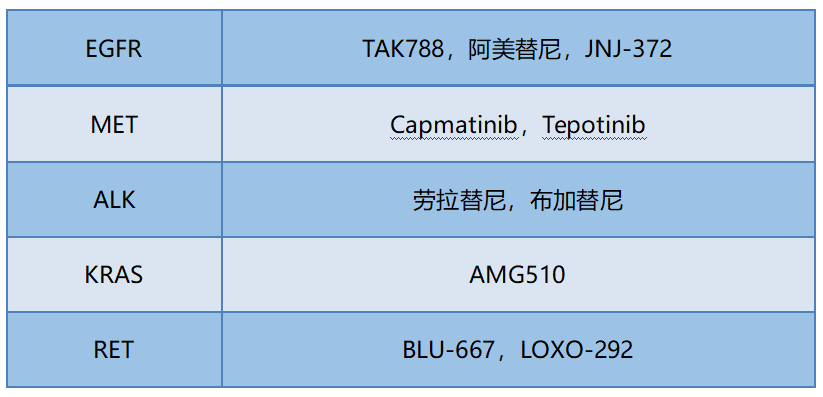
一(yī)、EGFR
1、TAK-788:治療EGFR20ins獲得突破性藥物(wù)資格!
EGFR20ins用現有的靶向藥治療效果并不理想,所幸新藥研發迅速。2020年(nián)04月27日,武田制藥公司宣布,美國(guó)FDA已授予其在研EGFR/HER2抑制劑TAK-788(Mobocertinib)突破性療法認定,用于治療接受含鉑化療期間(jiān)或之後病情進展的EGFR20插入突變的非小細胞肺癌(NSCLC)患者。
在劑量探索研究中,TAK-788治療EGFR/HER2 20ins及EGFR罕見(jiàn)突變NSCLC總人(rén)群的ORR(客觀緩解率)為(wèi)34.78%。無論既往是否接受過TKI或免疫治療,TAK-788都(dōu)可(kě)以展現出療效。最終确定的2期标準劑量(同時(shí)也是最大耐受劑量)為(wèi)160mg每天一(yī)次,口服。
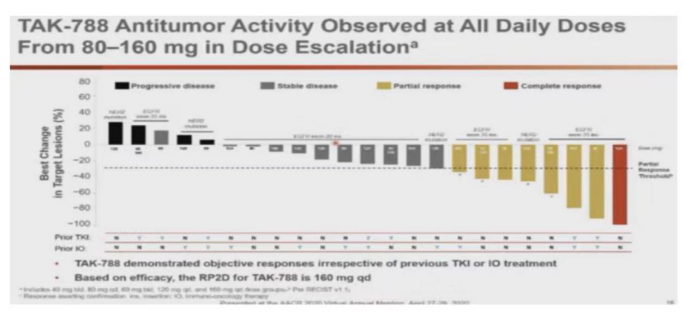
在隊列擴展研究中,28例可(kě)供評估的EGFR 20外(wài)顯子插入突變經治NSCLC患者,ORR為(wèi)43%,中位PFS(無進展生存期)為(wèi)7.3月。在不同EGFR20ins亞組突變患者中,都(dōu)可(kě)以觀察到療效。
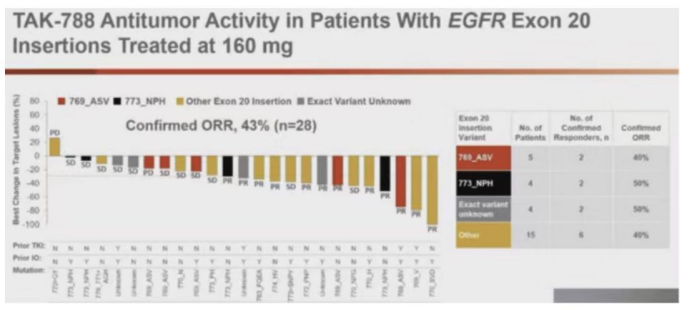
2、阿美替尼:首個上(shàng)市的國(guó)産第三代EGFR-TKI
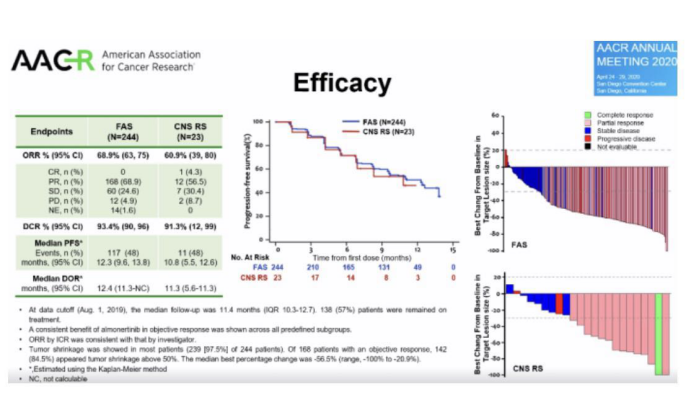
2020年(nián)3月18日,江蘇豪森藥業集團研發的三代EGFR靶向藥阿美替尼獲得國(guó)家藥監局批準上(shàng)市,用于既往EGFR-TKI治療進展且T790M陽性的晚期NSCLC患者的治療。該适應症獲批是基于APOLLO II期研究。給今年(nián)AACR大會更新的最新數(shù)據,該研究共分析了(le)244例患者,其中23例患者評估了(le)腦轉移療效。
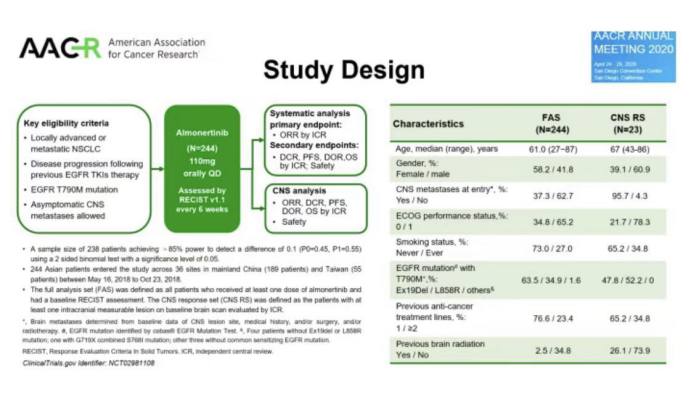
結果顯示,總人(rén)群的ORR為(wèi)68.9%,DCR為(wèi)93.4%,中位PFS為(wèi)12.3個月,中位DOR為(wèi)12.4個月。腦轉移療效評估,ORR為(wèi)60.9%,DCR為(wèi)91.3%,中位PFS為(wèi)10.8個月,中位DOR為(wèi)11.3個月。從(cóng)瀑布圖來看(kàn),總人(rén)群及腦轉移亞群的療效相似。
3、JNJ-372:治療20ins獲得FDA授予突破性療法
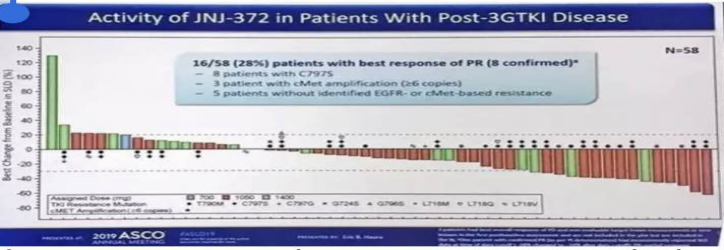
2020年(nián)3月11日,美國(guó)強生公司官網公布,其在研藥物(wù)JNJ-6372獲得FDA授予突破性療法認定,用于治療攜帶20外(wài)顯子插入突變(20ins)的EGFR陽性轉移性非小細胞肺癌(NSCLC)患者,這(zhè)些患者既往接受過鉑類化療且進展。這(zhè)是基于、第一(yī)階段試驗(NCT02609776)的結果的支持。1期研究納入了(le)108例經治的EGFR突變(包括敏感突變、20ins及其他(tā)罕見(jiàn)突變)晚期NSCLC患者,接受JNJ-372治療。
結果亮眼,在後線治療中,ORR達到了(le)30%之高,并且療效遍及各種EGFR亞型。這(zhè)些患者包括C797S突變,MET擴增,既往對奧希替尼耐藥。
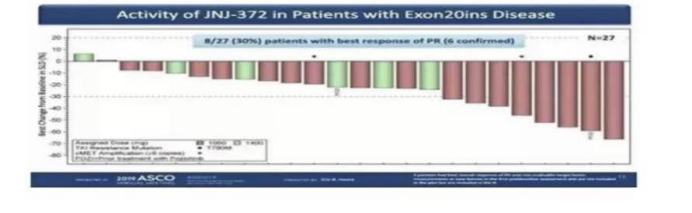
另外(wài),JNJ-372對EGFR20 ins還有起效。20ins亞組分析中,DCR居然達到100%!ORR為(wèi)30%(其中2例是波奇替尼耐藥的患者)。如(rú)此漂亮的數(shù)據給難治的20ins患者帶來新希望。
二、MET
1、Capmatinib:FDA獲批的首個MET抑制劑
Capmatinib為(wèi)諾華研發的MET高選擇性抑制劑。2020年(nián)5月6日,FDA加速批準Capmatinib用于治療MET14外(wài)顯子突變的非小細胞肺癌(NSCLC),比PDUFA日期提前了(le)3個月。Capmatinib成為(wèi)首個獲得FDA批準的MET抑制劑。在GEOMETRY II期研究中,納入了(le)MET 14 跳(tiào)躍突變或MET擴增的晚期NSCLC患者,接受Capmatinib進行(xíng)治療。隊列4(經治的患者,2/3線)研究結果顯示,BIRC評估的ORR為(wèi)40.6%,DCR為(wèi)78.3%,中位DOR為(wèi)9.72個月;研究者評估的ORR為(wèi)42%,DCR為(wèi)76.8%。
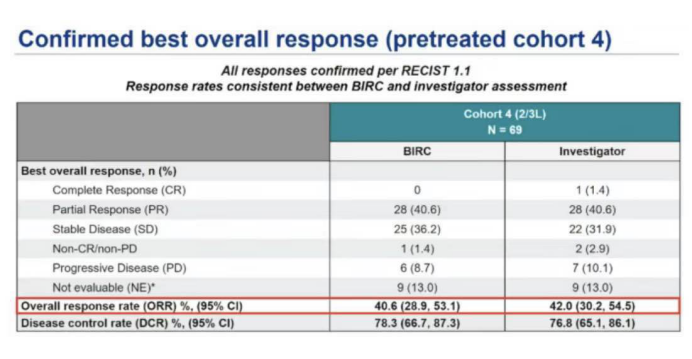
對于初治的患者(隊列5b),BIRC評估的ORR為(wèi)67.9%,DCR為(wèi)96.4%,中位DOR為(wèi)11.14個月;研究者評估的ORR為(wèi)60.7%,DCR為(wèi)96.4%。

對于13例出現腦轉移的MET 14突變患者,顱內(nèi)ORR達到了(le)54%(BIRC評估,7/13),其中4例所有腦轉移竈都(dōu)完全緩解,達到CR。
2、Tepotinib:日本上(shàng)市,全球首款MET抑制劑
2020年(nián)3月25日,日本厚生勞動省(MHLW)已批準tepotinib用于治療攜帶MET14号外(wài)顯子(MET ex14)跳(tiào)躍突變的晚期NSCLC患者。FDA也已經授予tepotinib突破性療法認定。該批準是基于ASCO 2019會議(yì)上(shàng)公布的正在進行(xíng)的VISION II期試驗初步數(shù)據。
研究中患者分别納入2個隊列:MET 外(wài)顯子14跳(tiào)過突變的患者和(hé) MET 擴增。在MET 外(wài)顯子14跳(tiào)躍突變隊列中,有73名患者的療效可(kě)評估,經液體活檢發現的患者,總ORR為(wèi)50%,DCR為(wèi)66.7%,中位DOR為(wèi)12.4個月;經組織活檢中發現的患者,總ORR為(wèi)45.1%,DCR為(wèi)72.5%,DOR中位數(shù)為(wèi)15.7個月。
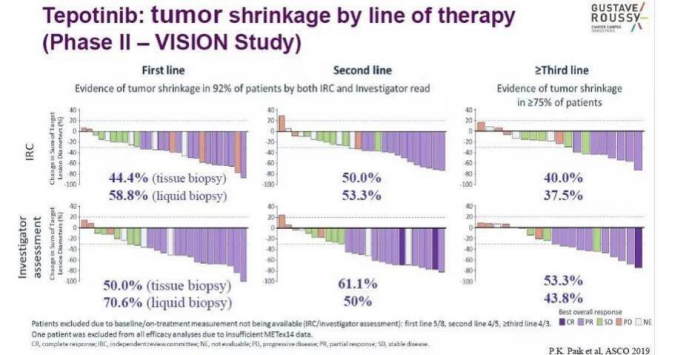
進一(yī)步分析了(le)不同治療線數(shù)的腫瘤緩解情況,可(kě)以看(kàn)出,無論是一(yī)線治療還是二線或三線治療,ORR都(dōu)可(kě)以達到40%-50%左右。緩解率并沒有随着治療線數(shù)的增加而降低(dī),并且對于二線及以上(shàng)治療的患者,ORR均可(kě)以達到45%以上(shàng),中位DOR則為(wèi)一(yī)年(nián)以上(shàng)甚至更長(cháng)。
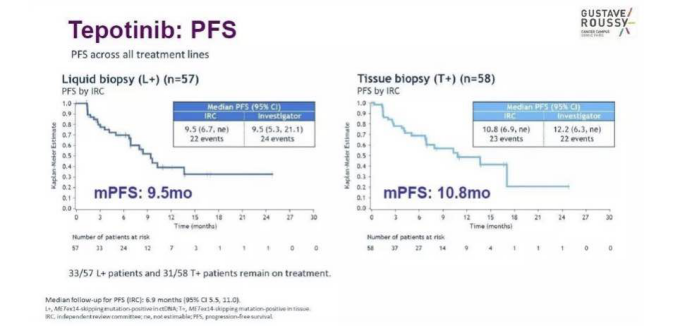
經液體活檢鑒定為(wèi)腫瘤的患者中,中位PFS為(wèi)9.5個月,而經組織活檢鑒定為(wèi)腫瘤的患者為(wèi)10.8個月。兩組的中位DOR為(wèi)14.3個月。
三、ALK
1、勞拉替尼:三代ALK抑制劑在香港上(shàng)市
2020年(nián)2月,輝瑞公司開(kāi)發的三代ALK抑制劑勞拉替尼,在香港獲批用于治療克唑替尼治療進展後或至少(shǎo)一(yī)種ALK抑制劑治療進展後;或阿來替尼瑞替尼作(zuò)為(wèi)首個ALK抑制劑治療進展後的ALK陽性晚期NSCLC患者。勞拉替尼獲批是基于一(yī)項I/II期臨床試驗(B7461001)結果。在ALK隊列共分析了(le)215例患者,最新數(shù)據顯示勞拉替尼治療的總人(rén)群ORR達到48%。
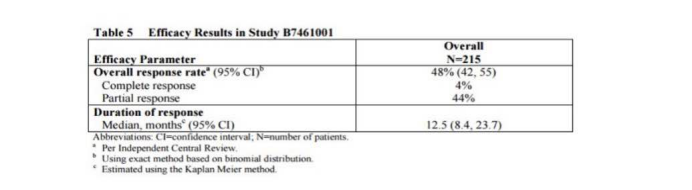
2018年(nián)ASCO報道(dào)的亞組分析顯示:
(1)對于初治的ALK陽性NSCLC患者,ORR達到90%,DCR達到97%;
(2)既往使用過克唑替尼或者克唑替尼+化療的患者,ORR高達69%;
(3) 對于使用過2-3種ALK抑制劑外(wài)加化療的患者,勞拉替尼作(zuò)為(wèi)三線甚至五線藥物(wù)使用,ORR依然達到39%。
總之,無論之前使用過幾種TKI靶藥或化療,勞拉替尼作(zuò)為(wèi)保底治療的療效都(dōu)非常不錯。

不僅如(rú)此,勞拉替尼治療腦轉移的顱內(nèi)ORR高達60%,中位DOR(緩解持續時(shí)間(jiān))為(wèi)19.5個月,為(wèi)ALK患者帶來強力且持久入腦的藥物(wù)。
2、布加替尼:在歐盟獲批一(yī)線,FDA也在審批該适應症
4月6日,武田宣布歐盟委員(yuán)會批準二代ALK-TKI布加替尼(brigatinib)新适應症,用于一(yī)線治療ALK+NSCLC患者。2月25日,該适應症也獲得了(le)FDA受理,并授予其優先評審資格。

布加替尼的一(yī)線适應症申請(qǐng)是基于ALTA-1L研究結果。該III期随機多中心試驗納入了(le)275例既往未接受過靶向治療的ALK陽性晚期NSCLC患者,接受布加替尼或一(yī)代ALK-TKI(靶向藥)克唑替尼治療。去年(nián)ESMO ASIA大會更新了(le)研究結果。布加替尼組的BIRC(獨立評審中心評估)中位PFS達到24個月,碾壓克唑替尼的11個月,翻了(le)超過一(yī)倍!研究者評估的PFS,布加替尼達到了(le)29.4個月,而克唑替尼隻有9.2個月。

重要(yào)的是,布加替尼入腦效果驚人(rén)。對于腦轉移患者,布加替尼組的BIRC中位PFS達到了(le)24個月,而克唑替尼隻有5.6個月。布加替尼的控腦能(néng)力明(míng)顯優于克唑。

四、KRAS
1、AMG510:突破KRAS困境,獲得孤兒藥資格
作(zuò)為(wèi)成功改寫曆史的首款KRAS抑制劑,安進公司的AMG510獲得了(le)FDA授予的治療KRASG12C突變陽性NSCLC和(hé)結直腸癌的孤兒藥資格。今年(nián)ASCO、WCLC和(hé)ESMO三大腫瘤會議(yì)上(shàng),安進公司公布了(le)KRAS靶藥AMG510正在進行(xíng)的1期研究新數(shù)據。該研究評估了(le)AMG 510在先前治療過的KRAS G12C突變的實體瘤患者(包括結直腸癌,闌尾癌和(hé)NSCLC患者)中的安全性和(hé)療效。
NSCLC患者的總ORR為(wèi)48%,DCR為(wèi)96%。在13名接受劑量為(wèi)960 mg AMG 510的NSCLC患者中,ORR為(wèi)54%,DCR為(wèi)100%。

五、RET
1、BLU-667:首個國(guó)産RET抑制劑即将在國(guó)內(nèi)上(shàng)市,有效率可(kě)高達71%
Pralsetinib(BLU-667)是一(yī)種口服、強效且對RET融合和(hé)突變(含耐藥突變)具有高選擇性的RET抑制劑。近日,基石藥業也宣布了(le)該藥的I/II期試驗已完成中國(guó)最後一(yī)例的NSCLC患者入組,計劃在2020年(nián)下(xià)半年(nián)在國(guó)內(nèi)遞交新藥上(shàng)市申請(qǐng)。目前,BLU-667已經向FDA提交新藥上(shàng)市申請(qǐng)。
在2019ASCO公布的I/II期試驗數(shù)據中,有48例可(kě)評估療效的RET融合NSCLC患者(初治或經治)接受BLU-667治療。總ORR為(wèi)58%,DCR達到96%。既往做(zuò)過鉑類化療患者(n=35)的ORR為(wèi)60%,DCR為(wèi)100%。另外(wài),初治患者的ORR為(wèi)71%(5/7)。中位DOR未達到,PFS和(hé)OS未達到,還有82%患者在用BLU-667治療。腦轉移療效方面,顱內(nèi)ORR為(wèi)78%(7/9),高效入腦。

2、LOXO-292:RET靶向新星,顱內(nèi)有效率高達91%!
2020年(nián)1月30日,禮來公司宣布其RET抑制劑selpercatinib(LOXO-292)已獲得美國(guó)FDA授予的優先審評資格,有望加速獲批治療攜帶RET融合陽性NSCLC晚期患者。
LOXO-292作(zuò)為(wèi)RET靶向藥,近期開(kāi)展了(le)全球首個RET選擇性抑制劑的III期研究。在前期LIBRETTO-001這(zhè)項1/2期研究中,納入了(le)RET融合的晚期NSCLC患者,使用LOXO292(Selpercatinib)進行(xíng)治療。結果顯示,總人(rén)群的ORR達到68%,DCR為(wèi)94%。對于腦轉移患者,ORR為(wèi)91%,DCR為(wèi)100%!可(kě)見(jiàn),LOXO292不僅高效,入腦能(néng)力還非常強。中位DOR為(wèi)20.3個月,中位PFS為(wèi)18.4個月。療效非常持久。

将LOXO292與國(guó)産RET抑制劑BLU667(pralsetinib)進行(xíng)對比,兩者療效都(dōu)相當不錯。

聲明(míng):本資料中涉及的信息僅供參考,請(qǐng)遵從(cóng)醫(yī)生或其他(tā)醫(yī)療衛生專業人(rén)士的意見(jiàn)或指導。
本文版權歸找藥寶典所有,任何個人(rén)或機構轉載需獲得找藥寶典授權,在授權範圍內(nèi)使用,并标注來源“找藥寶典”。
文章(zhāng)轉載、媒體合作(zuò)請(qǐng)聯系小編:p88128812