本文系J Control Release原創,首發平台J Control Release微(wēi)信公衆号。
近日,吉林大學藥學院韓冰教授團隊在《Journal of Controlled Released》期刊2023年(nián)第353期上(shàng)以題為(wèi)“Mucus
adhesion vs. mucus penetration? Screening nanomaterials for nasal inhalation by
MD simulation”發表了(le)研究型論文。
經鼻給藥具有吸收迅速、非侵入性與可(kě)繞過血腦屏障等優勢,已在中樞神經系統疾病的藥物(wù)遞送應用中取得許多進展。采用納米載體可(kě)以改善藥物(wù)在鼻-腦遞送途徑中的吸收與滲透,具有代表性的黏膜輸送系統:粘液粘附性納米粒子(MAPs)與粘液滲透性納米粒子(MPPs),常用于遞送藥物(wù)。
這(zhè)兩種看(kàn)似矛盾的性質均在經鼻給藥時(shí)發揮作(zuò)用,然而具體的作(zuò)用機理有待于闡明(míng)。此外(wài),在鼻腔的環境下(xià),經典的藥物(wù)載體在鼻吸入遞送時(shí)産生的效力并非最佳,載體材料仍然需要(yào)進一(yī)步的優化。
人(rén)體濕潤的上(shàng)皮表面都(dōu)覆蓋粘液層,其動态彈性凝膠網狀結構将給納米藥物(wù)的遞送帶來挑戰。粘液層的關鍵性功能(néng)組分是粘蛋白,分泌性黏蛋白MUC5AC對呼吸道(dào)粘液凝膠網絡的性質起調控作(zuò)用。在合理設計更有效的藥物(wù)遞送納米系統時(shí),需要(yào)考慮納米尺寸的載體與粘蛋白網絡的相互作(zuò)用情況,确定納米載體與粘液蛋白之間(jiān)的作(zuò)用的特征。
分子動力學(Molecular dynamics ,MD)模拟揭示其全原子動力學特征與相互作(zuò)用細節,從(cóng)而幫助理解納米載體在遞送中的過程。該研究利用GROMACS進行(xíng)MD模拟,以探究人(rén)MUC5AC(hMUC5AC)與MAPs(殼聚糖: COS、2-羟丙基三甲基氯化铵殼聚糖: HTCC)及MPPs(聚乙二醇化聚合物(wù):PEG-PLGA與PEG-PLA)的互作(zuò)機制,從(cóng)而建立有效的藥物(wù)經鼻遞送系統的載體篩選平台。
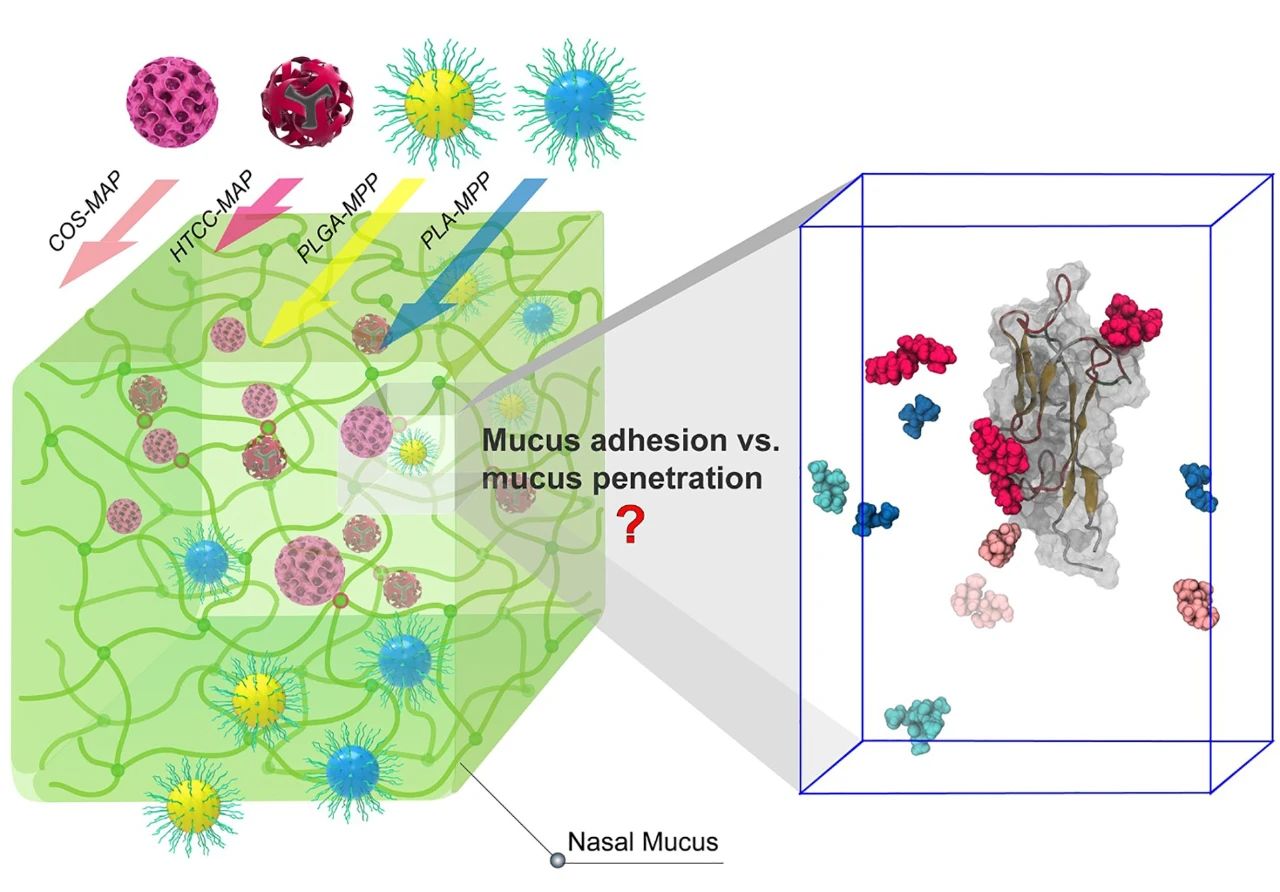
圖1. MD模拟MAPs和(hé)MPPs與鼻粘液蛋白的相互作(zuò)用
該研究通(tōng)過均方根偏差(RMSD)和(hé)均方根波動(RMSF)探究了(le)構建的hMUC5AC與NPs複合體系的穩定性與構象變化。為(wèi)了(le)探究hMUC5AC在模拟過程中的折疊細節與親疏水效應,該研究統計了(le)各體系的溶劑可(kě)及表面積(SASA),發現hMUC5AC-PEG-PLGA體系的數(shù)值發生了(le)較大變異(圖2),其峰值暗示模拟終末段hMUC5AC緊密構象的解聚與展開(kāi)(圖2),使其疏水相互作(zuò)用受到影響,進而改變複合體系流變學特性,使其具有粘液滲透性。基于DSSP的二級結構分析也獲得了(le)與SASA分析一(yī)緻的結果。
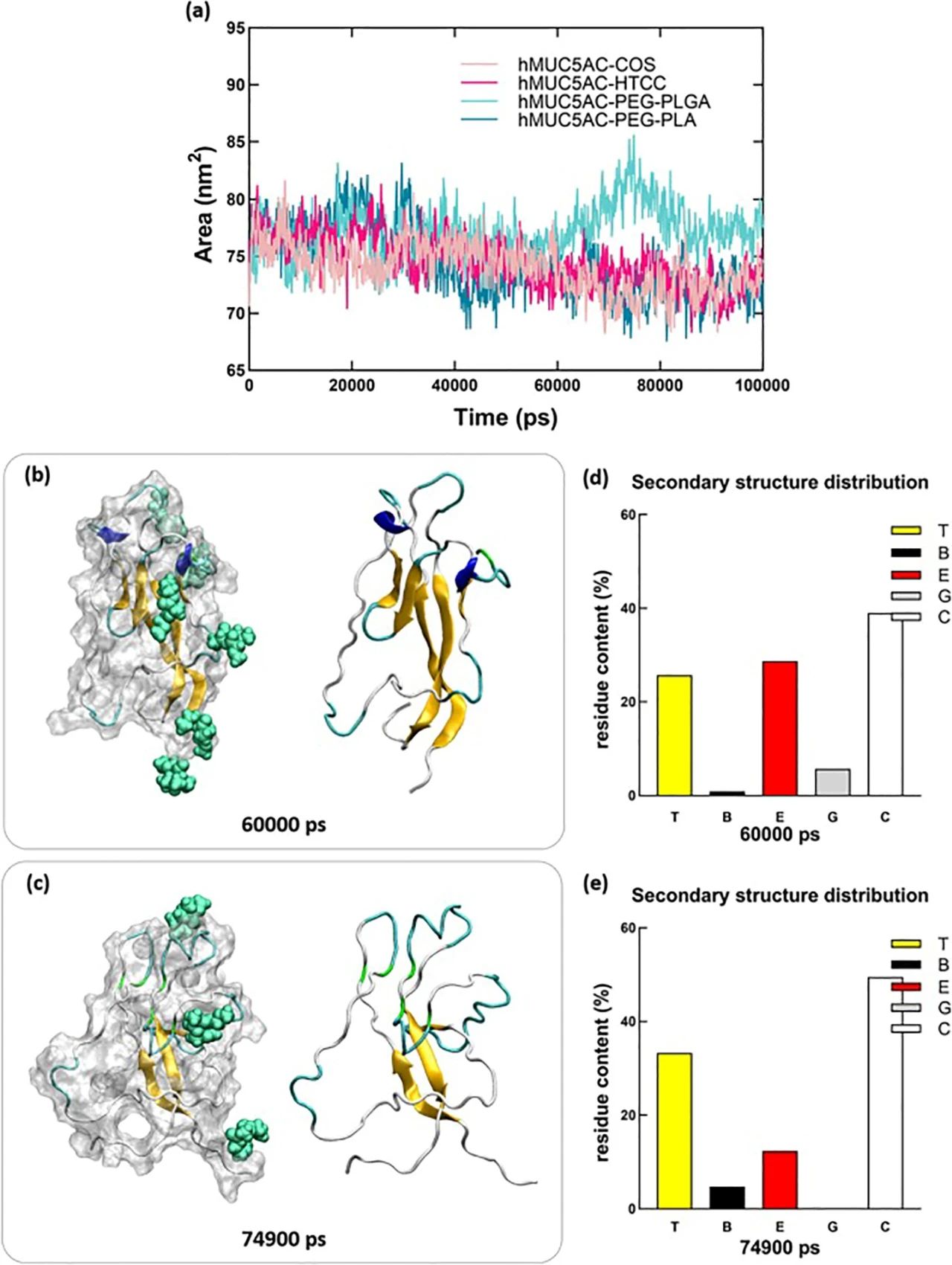
圖2.各體系SASA (a)與hMUC5AC-PEG-PLGA體系在峰值前(b)與峰值處(c)的蛋白構象,并對其二級結構進行(xíng)了(le)分析(d,e)為(wèi)了(le)進一(yī)步對比四種類型的納米材料與MUC5AC之間(jiān)的相互作(zuò)用情況,該研究還統計了(le)hMUC5AC與NPs的碰撞次數(shù)。MAPs的碰撞次數(shù)顯著高于MPPs, HTCC在整個模拟過程中與hMUC5AC高頻(pín)碰撞,暗示HTCC具有粘膜黏附特性。
為(wèi)了(le)更好的确定hMUC5AC與納米材料的互作(zuò)細節,該研究對各體系的高頻(pín)碰撞特征時(shí)點進行(xíng)了(le)分析,并用PLIP确定其非鍵相互作(zuò)用類型。MAPs與hMUC5AC存在多處穩定的作(zuò)用位點,其中HTCC的季胺基與粘蛋白殘基Asp12形成鹽橋(圖3b),這(zhè)與其所具有的強電荷吸附作(zuò)用相一(yī)緻。而MPPs整體缺乏與hMUC5AC穩定的相互作(zuò)用形式,表現出粘液滲透特性。
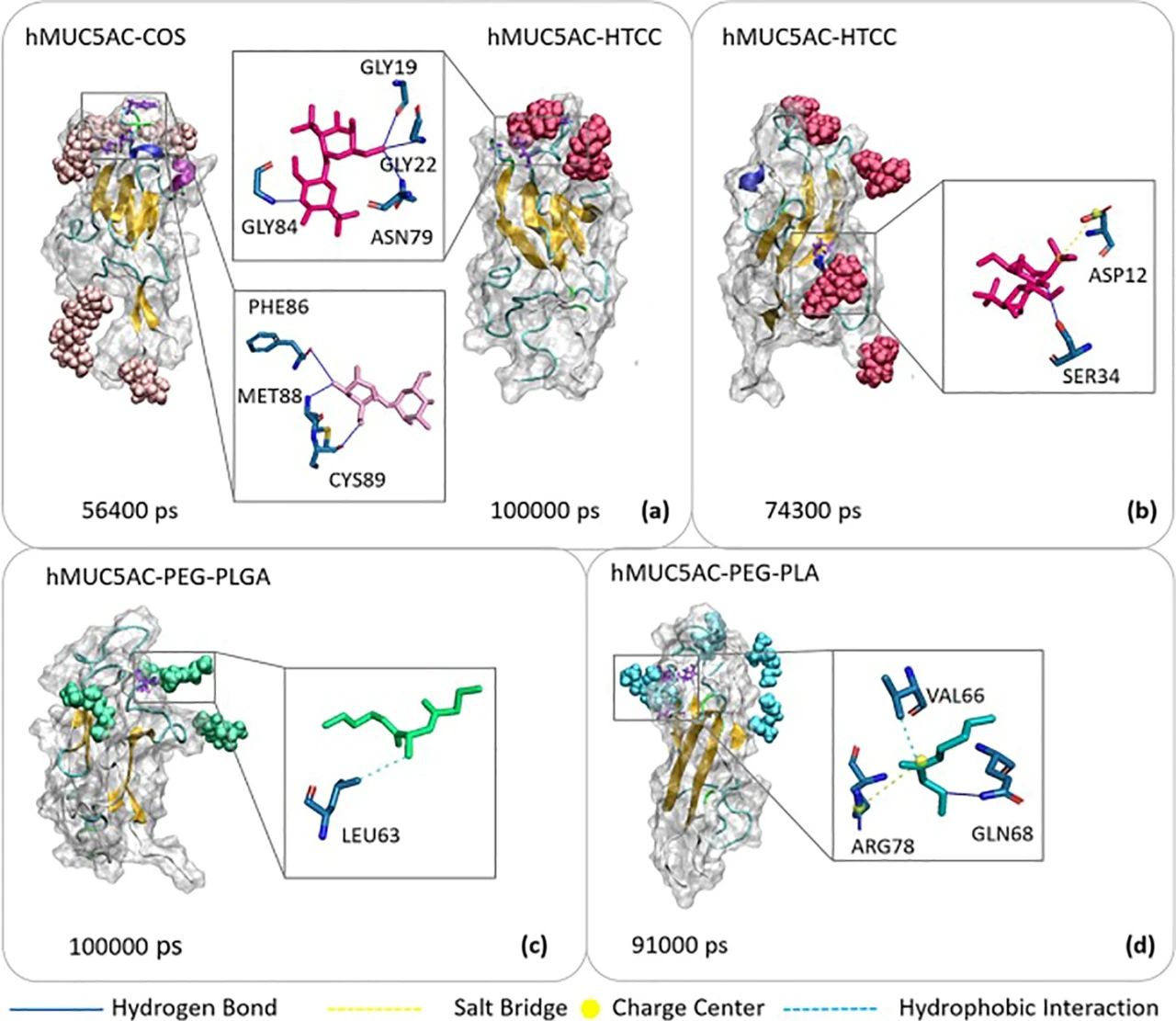
圖3 .四體系特征時(shí)點的非共價相互作(zuò)用分析
綜合來看(kàn),由hMUC5AC與NPs的MD模拟結果可(kě)得,四體系中相互作(zuò)用的強度順序依次為(wèi):hMUC5AC-HTCC>hMUC5AC-COS>hMUC5AC-PEG-PLA>hMUC5AC-PEG-PLGA。這(zhè)一(yī)結論在後續實驗中也得到了(le)驗證。
該研究在MD模拟基礎上(shàng)進行(xíng)了(le)體外(wài)、離體實驗的材料篩選及功能(néng)驗證。該研究在統一(yī)粒徑尺寸的條件下(xià)開(kāi)展了(le)研究工(gōng)作(zuò),并控制NPs處于相對規則和(hé)均勻的形态,避免形狀引起的任何影響,以研究NPs的不同性質與粘液中粘蛋白之間(jiān)的相互作(zuò)用。
受MD模拟結果的啓發,該研究團隊利用比濁法對NPs與hMUC5AC的結合親和(hé)力進行(xíng)了(le)體外(wài)驗證。随者粘蛋白濃度的增加,MAPs與粘蛋白的混合物(wù)的濁度也表現出協同增加,表明(míng)MAPs和(hé)粘蛋白的聚集。
在MAPs中,ΔA>>0,表明(míng)其間(jiān)存在着強烈的相互作(zuò)用,其中HTCC的斜率值更大,表明(míng)其相互作(zuò)用更顯著。然而,MPPs與粘蛋白的濁度變化則無此正相關性,表明(míng)後者與粘蛋白的親和(hé)力弱,不能(néng)使粘蛋白發生聚集。随後,該團隊進一(yī)步利用Transwell法測定了(le)NPs的粘液滲透性能(néng),并發現MPPs的粘液穿透性明(míng)顯優于MAPs,且PEG-PLGA的滲透效率顯著高于PEG-PLA(圖4),與MD模拟分析的結論一(yī)緻。
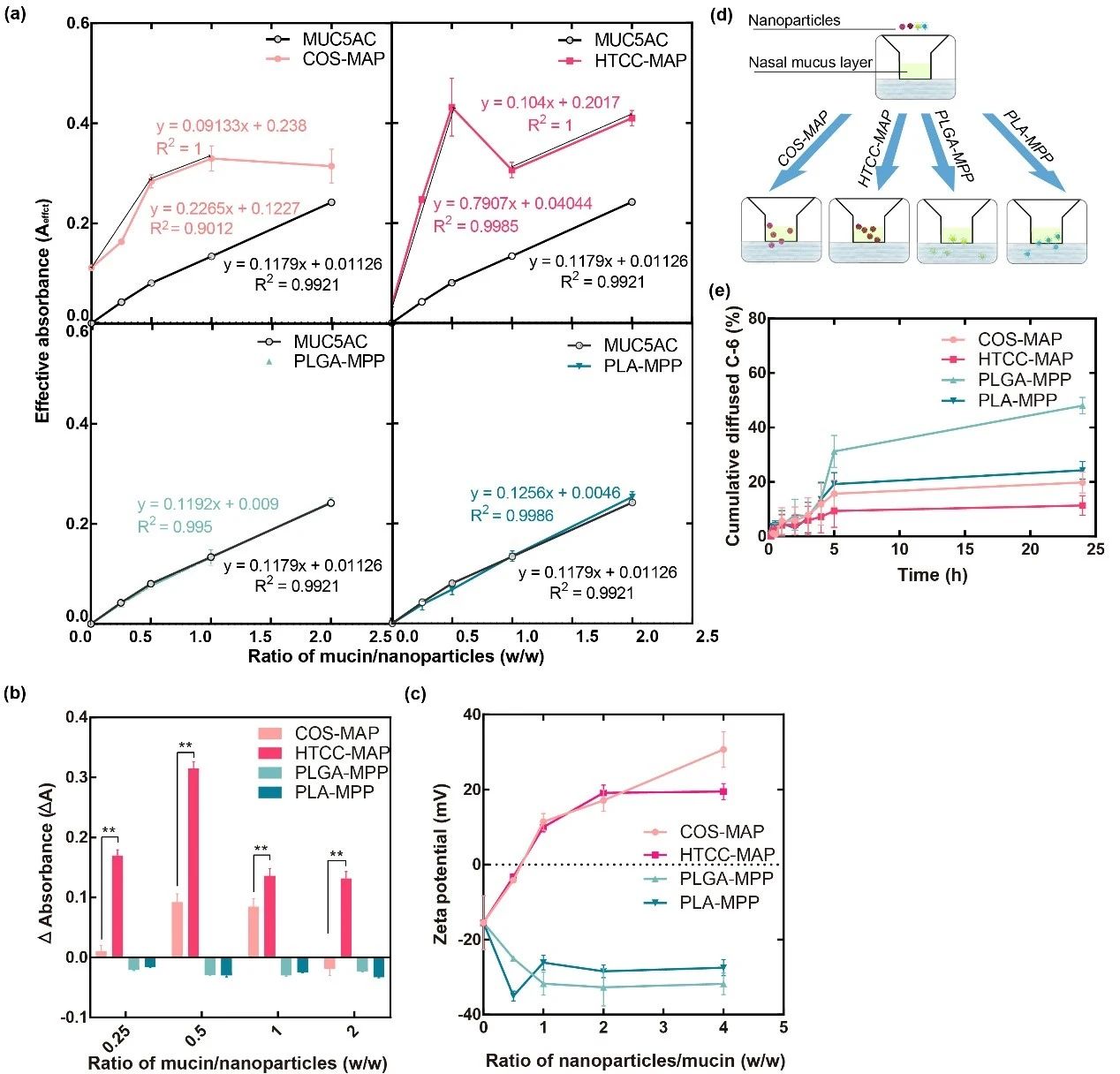
圖4. MAPs與MPPs與粘蛋白的不同作(zuò)用性質 (a-c)濁度法測量不同NPs與粘蛋白的結合親和(hé)力(d-e) Transwell法測定不同NPs的粘液滲透性能(néng)理想的載體材料不僅應幫助藥物(wù)快(kuài)速通(tōng)過粘彈性凝膠層,還應在粘膜內(nèi)順利擴散以更深入地(dì)輸送藥物(wù)。為(wèi)研究不同NPs在鼻黏膜中的擴散性能(néng),該研究利用改進的Valia-Chien擴散池,選用豬鼻嗅黏膜進行(xíng)離體實驗,發現MPPs的粘膜穿透效率明(míng)顯高于MAPs,與前文研究一(yī)緻。這(zhè)為(wèi)跨粘膜給藥途徑的實際應用提供了(le)實驗數(shù)據參考。
MAPs藥物(wù)載體因其粘液粘附性而具有更長(cháng)的給藥保留時(shí)間(jiān),但(dàn)MAPs多數(shù)與黏液蛋白産生較強的靜電作(zuò)用和(hé)氫鍵,往往被固定在粘液屏障中,由于鼻腔粘液的高周轉率,使納米藥物(wù)存在被清除的風(fēng)險,故此時(shí)采用MPPs或具有一(yī)定優勢。
對MAPs與MPPs矛盾特性的組合應用或更有利于提高經鼻給藥納米藥物(wù)的生物(wù)利用度。基于MD模拟的納米載體篩選平台能(néng)揭示不同性質的NPs與粘蛋白網絡相互作(zuò)用的特征,輔助對比具有相似性質的NPs在藥物(wù)遞送時(shí)的細微(wēi)差異,為(wèi)經鼻給藥的納米藥物(wù)遞送載體的設計提供新的見(jiàn)解。
亮點總結
1、對鼻腔內(nèi)粘液屏障進行(xíng)模拟、并将其作(zuò)為(wèi)經鼻給藥的納米載體篩選平台;
2、将MD模拟和(hé)體外(wài)、離體實驗相結合、對納米藥物(wù)載體進行(xíng)篩選;
3、闡明(míng)了(le)MAPs與MPPs經粘液凝膠網格的藥物(wù)遞送機制;
4、利用MD模拟描述了(le)納米載體與粘膜屏障的相互作(zuò)用細節;
5、為(wèi)經鼻給藥納米遞送載體的設計提供新見(jiàn)解。
文章(zhāng)信息
Volume 353, January 2023, Pages 366-379
https://doi.org/10.1016/j.jconrel.2022.11.051
作(zuò)者信息
通(tōng)訊作(zuò)者:
蔣振彥,主要(yào)研究領域為(wèi)生物(wù)物(wù)理化學,研究方向主要(yào)包括膜蛋白的構像變化動力學及生物(wù)功能(néng),神經系統信号傳導等。結合熒光(guāng)共振能(néng)量轉移和(hé)生物(wù)化學方法,研究GPCR,EGFR,TLR4等調控的結構基礎和(hé)詳細的生物(wù)化學過程;解析相關的信号通(tōng)路中的蛋白質複合物(wù)變構機制,給出相關過程分子機制的詳細圖像,從(cóng)而為(wèi)相關疾病治療藥物(wù)設計提供線索。結合化學生物(wù)學和(hé)計算生物(wù)學方法研究轉運體等膜蛋白體系中蛋白質的構象動力學性質,以及底物(wù)輸運的能(néng)量信息,揭示構象動力學對蛋白質功能(néng)調控的意義,為(wèi)解決相關疾病治療藥物(wù)的耐藥性問(wèn)題提供思路。
韓冰,吉林大學藥學院教授,博士生導師(shī),主要(yào)研究領域為(wèi)藥物(wù)制劑學。研究方向主要(yào)包括五官科給藥的遞送行(xíng)為(wèi)研究,以及神經退行(xíng)性疾病和(hé)腫瘤疾病的藥物(wù)遞送研究等。主持科技部中小企業創新基金(jīn),國(guó)家自(zì)然科學基金(jīn),省級科技發展基金(jīn)等十餘項,兩次獲吉林省科學技術(shù)進步二等獎。
【參考資料】
[1] Agrawal M, et al. Nose-to-brain
drug delivery: An update on clinical challenges and progress towards approval
of anti-Alzheimer drugs[J]. Journal of controlled release, 2018, 281: 139-177.
[2]
Garcia-Diaz M, et al. The role of mucus as an invisible cloak to
transepithelial drug delivery by nanoparticles[J]. Advanced drug delivery
reviews, 2018, 124: 107-124.
[3] Pai R V, et al. Exploring molecular dynamics
simulation to predict binding with ocular mucin: An in silico approach for
screening mucoadhesive materials for ocular retentive delivery systems[J].
Journal of Controlled Release, 2019, 309: 190-202.
翻譯 | 熊茵
校對 | 高小舒
排版 | 王海(hǎi)瑞




