
引言
近年(nián)來,License out模式已成為(wèi)中國(guó)創新藥企業“借船(chuán)出海(hǎi)”的重要(yào)選擇,創新藥企業License out交易日趨活躍,交易數(shù)量、金(jīn)額及項目種類方面呈逐年(nián)增高态勢。2023年(nián)上(shàng)半年(nián)中國(guó)生物(wù)醫(yī)藥License out交易TOP10事件的交易總額達117.833億美元。從(cóng)交易金(jīn)額看(kàn),共有6起License out交易金(jīn)額突破10億美元,單項最高交易金(jīn)額達20億美元,為(wèi)百力司康與衛材關于BB-1701的合作(zuò)協議(yì)。
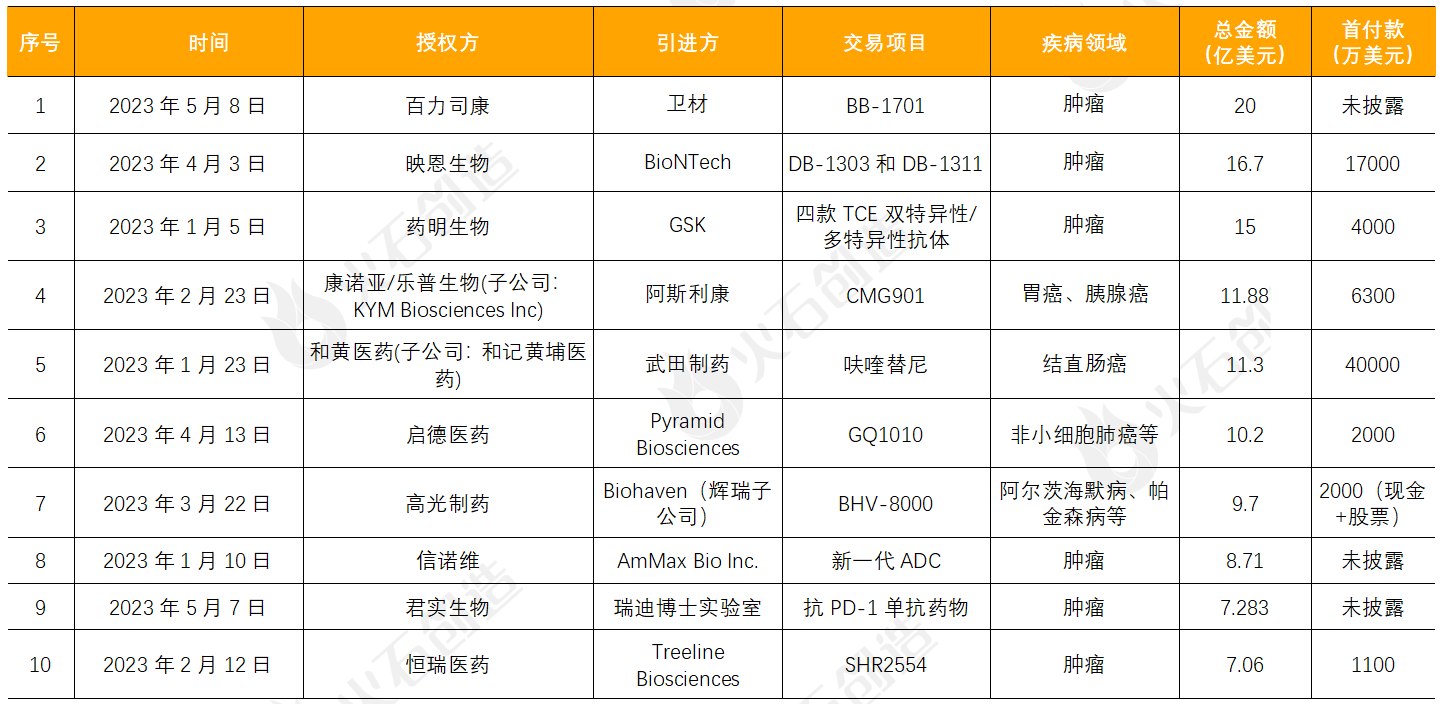
2023年(nián)5月8日,緻力于開(kāi)發差異化抗體偶聯藥(ADC)的臨床階段生物(wù)醫(yī)藥公司百力司康宣布與衛材株式會社就BB-1701達成具有戰略合作(zuò)選擇權的臨床試驗合作(zuò)協議(yì)。根據協議(yì),百力司康将獲得首付款和(hé)裏程碑付款,百力司康和(hé)衛材将就BB-1701進行(xíng)共同開(kāi)發。如(rú)衛材行(xíng)使BB-1701戰略合作(zuò)的選擇權,百力司康會獲得相應的行(xíng)權付款,同時(shí)将獲得總計高達20億美元的開(kāi)發與商業化裏程碑付款, 以及銷售分成,衛材會獲得BB-1701的全球(除大中華區(qū)外(wài))開(kāi)發和(hé)商業化權益。
BB-1701是一(yī)款由百力司康開(kāi)發的以艾立布林為(wèi)毒素的治療癌症的人(rén)表皮生長(cháng)因子受體-2(HER2)ADC創新藥,旨在為(wèi)局部晚期和(hé)轉移性HER2陽性實體瘤患者提供更加安全有效的治療方案, 具有應用于多種腫瘤适應症的市場前景。BB-1701具有獨特的作(zuò)用機制(MOA),包括有效的旁路殺傷效應以及免疫原性細胞死亡(ICD)活性,目前正在進行(xíng)中美I/II期國(guó)際多中心臨床試驗,已有上(shàng)百例不同癌種患者用藥。
2023年(nián)4月3日,專注于發現和(hé)開(kāi)發下(xià)一(yī)代抗體偶聯藥物(wù)(ADC)以治療癌症和(hé)自(zì)身免疫性疾病患者的臨床階段生物(wù)技術(shù)公司映恩生物(wù)(DualityBio)宣布就兩款ADC産品(DB-1303和(hé)DB-1311)與BioNTech簽訂獨家許可(kě)和(hé)合作(zuò)協議(yì),BioNTech将獲得在全球範圍內(nèi)開(kāi)發、制造和(hé)商業化這(zhè)兩款ADC(不包括中國(guó)大陸,香港特别行(xíng)政區(qū)和(hé)澳門特别行(xíng)政區(qū))的權利。
根據協議(yì)條款,映恩生物(wù)将獲得總計1.7億美元的首付款,以及兩款ADC産品的開(kāi)發、監管和(hé)商業裏程碑付款,總額可(kě)能(néng)超過15億美元。映恩生物(wù)還将有資格從(cóng)兩款ADC産品的淨銷售額中獲得高達低(dī)雙位數(shù)的分層特許權使用費(fèi)。
DB-1303是一(yī)種基于拓撲異構酶-1抑制劑的ADC候選藥物(wù),針對人(rén)表皮生長(cháng)因子受體2(HER2),該靶标在多種癌症中過度表達,有助于癌細胞的侵襲性生長(cháng)和(hé)擴散。靶向HER2的抗體療法已被證明(míng)是表達HER2的癌症的有效治療策略。DB-1303是由映恩生物(wù)專有的Duality免疫毒素抗體偶聯物(wù)(DITAC)平台構建的第三代HER2 ADC産品,在HER2陽性和(hé)HER2低(dī)表達細胞和(hé)腫瘤模型中均表現出有效的抗腫瘤活性,具有良好的安全性和(hé)可(kě)能(néng)擴大的治療窗口。DB-1303項目獲得了(le)美國(guó)食品和(hé)藥物(wù)管理局(“FDA”)的快(kuài)速通(tōng)道(dào)指定,目前正在進行(xíng)2期臨床試驗(NCT05150691),用于表達HER2的晚期實體瘤。
DB-1311同樣是基于拓撲異構酶-1抑制劑的ADC候選藥物(wù)之一(yī),是一(yī)款由映恩生物(wù)專有的DITAC接頭有效載荷組成的ADC。它在代表多種癌症類型的一(yī)系列腫瘤模型中表現出有效的抗腫瘤活性,并且在臨床前研究中具有良好的耐受性,具有良好的藥代動力學特征。臨床前抗腫瘤活性及其安全性所證明(míng)的寬治療窗口支持DB-1311解決各種癌症中未滿足的醫(yī)療需求的潛力。
2023年(nián)1月5日,全球領先的合同研究、開(kāi)發和(hé)生産(CRDMO)服務公司藥明(míng)生物(wù)宣布與葛蘭素史克(GSK)達成許可(kě)協議(yì),GSK将獲得基于藥明(míng)生物(wù)專利技術(shù)平台開(kāi)發的至多四款TCE雙特異性/多特異性抗體的獨家權利。
根據協議(yì),GSK将獲得一(yī)款處于臨床前階段的雙特異性抗體和(hé)其他(tā)至多三款處于早期發現階段的TCE抗體的全球獨家研究、開(kāi)發、生産和(hé)商業化權利。該款雙抗分别靶向腫瘤細胞表面的腫瘤相關抗原(TAA)和(hé)T細胞表面抗原CD3,通(tōng)過與腫瘤細胞及T細胞結合,特異性激活T細胞,從(cóng)而殺傷腫瘤細胞,産生抗腫瘤活性。藥明(míng)生物(wù)将獲得4000萬美元首付款和(hé)最高達14.6億美元的四款TCE抗體的研究、開(kāi)發、注冊和(hé)商業化裏程碑付款。藥明(míng)生物(wù)也有資格獲得基于淨銷售額的分級銷售提成。
WuXiBody®是藥明(míng)生物(wù)具有自(zì)主知識産權的雙特異性抗體技術(shù)平台。該平台突破了(le)絕大多數(shù)雙特異性抗體平台技術(shù)瓶頸,具有表達量高、穩定性高、溶解度好、易于純化等優勢,并且能(néng)夠為(wèi)每個項目節約6到18個月研發時(shí)間(jiān)以及顯著降低(dī)雙特異性抗體生産成本。WuXiBody®平台幾乎可(kě)将所有抗體序列用以構建雙特異性抗體,并且有望降低(dī)免疫原性風(fēng)險及延長(cháng)其體內(nèi)半衰期。WuXiBody®平台還兼具獨特的靈活性,可(kě)以構建各種不同的價數(shù)(如(rú)二價、三價或四價雙特異性抗體),以滿足不同項目的生物(wù)學特性需求。
2023年(nián)2月23日,阿斯利康與 KYM Biosciences Inc.已就潛在世界首創靶向Claudin 18.2的抗體偶聯藥物(wù)(ADC)CMG901達成全球獨家授權協議(yì)。Claudin 18.2是一(yī)個有前景的胃癌治療靶點。根據授權協議(yì),阿斯利康将負責CMG901的全球研發、制造和(hé)商業化。基于此協議(yì)及條款,由樂(yuè)普生物(wù)和(hé)康諾亞合資設立的KYM
Biosciences Inc.将獲得6300萬美元的預付款和(hé)超過11億美元的潛在額外(wài)研發和(hé)銷售相關的裏程碑付款,以及高達低(dī)雙位數(shù)的分層特許權使用費(fèi)。阿斯利康将獲得 CMG901 研究、開(kāi)發、注冊、生産和(hé)商業化的獨家全球許可(kě)。該交易預計于 2023 年(nián)上(shàng)半年(nián)完成,具體取決于慣例成交條件和(hé)監管許可(kě)。
CMG901 是首個在中國(guó)及美國(guó)均取得臨床研究申請(qǐng)批準的靶向 Claudin 18.2 的全新重組人(rén)源化單克隆抗體偶聯藥物(wù),由抗 Claudin
18.2單克隆抗體、可(kě)裂解的鏈接體和(hé)細胞毒性小分子單甲基澳瑞他(tā)汀E (MMAE)組成。CMG901正被開(kāi)發用于包括胃癌在內(nèi)的細胞表面表達 Claudin18.2 蛋白的實體腫瘤的治療。CMG901由KYM Biosciences Inc.(KYM)所有,KYM 是康諾亞(KYM
70%的所有權)和(hé)樂(yuè)普生物(wù)(KYM 30%的所有權)成立的合資企業。
2023年(nián)1月23日,和(hé)黃(huáng)醫(yī)藥(中國(guó))有限公司宣布其子公司和(hé)記黃(huáng)埔醫(yī)藥(上(shàng)海(hǎi))有限公司與武田制藥達成獨家許可(kě)協議(yì),在除中國(guó)內(nèi)地(dì)、香港和(hé)澳門以外(wài)的全球範圍內(nèi)進一(yī)步推進呋喹替尼的開(kāi)發、商業化和(hé)生産。呋喹替尼在中國(guó)內(nèi)地(dì)、香港和(hé)澳門由和(hé)黃(huáng)醫(yī)藥銷售。和(hé)記黃(huáng)埔醫(yī)藥(上(shàng)海(hǎi))有限公司将獲得總額高達11.3億美元的付款,其中包括協議(yì)完成時(shí)4億美元的首付款,以及潛在的監管注冊、開(kāi)發和(hé)商業銷售裏程碑付款,并外(wài)加基于淨銷售額的特許權使用費(fèi)。該項協議(yì)計劃于2023年(nián)完成在美國(guó)、歐洲和(hé)日本的上(shàng)市許可(kě)申請(qǐng)提交。該交易的生效取決于一(yī)些慣例性成交條件,包括完成反壟斷監管審查。在滿足這(zhè)些條件後,武田制藥将全權負責呋喹替尼在除中國(guó)內(nèi)地(dì)、香港和(hé)澳門以外(wài)的全球所有地(dì)區(qū)的開(kāi)發和(hé)商業化。
與此同時(shí),和(hé)黃(huáng)醫(yī)藥将繼續與禮來公司合作(zuò),專注于推進呋喹替尼在中國(guó)內(nèi)地(dì)的後期臨床試驗和(hé)商業化。呋喹替尼在中國(guó)內(nèi)地(dì)已獲批,并以商品名愛優特®上(shàng)市銷售,用于治療既往接受過氟嘧啶、奧沙利鉑和(hé)伊立替康治療的轉移性結直腸癌患者,包括既往接受過抗血管內(nèi)皮生長(cháng)因子(“VEGF”)治療和(hé)/或抗表皮生長(cháng)因子受體(“EGFR”)治療(RAS野生型)的患者。愛優特®自(zì)2020年(nián)1月起獲納入中國(guó)國(guó)家醫(yī)保藥品目錄。
呋喹替尼是一(yī)種高選擇性、強效的血管內(nèi)皮生長(cháng)因子受體(“VEGFR”)-1、-2及-3抑制劑。呋喹替尼可(kě)通(tōng)過口服給藥,并有潛力用于轉移性結直腸癌的各種亞型中且不受生物(wù)标志物(wù)狀态影響。呋喹替尼用于治療難治性轉移性結直腸癌患者的FRESCO-2國(guó)際多中心III期臨床試驗已取得積極結果,并于2022年(nián)9月舉行(xíng)的歐洲腫瘤內(nèi)科學會(“ESMO”)年(nián)會上(shàng)公布。FRESCO-2研究在轉移性結直腸癌患者中達到了(le)改善總生存期(“OS”)的主要(yào)研究終點,且一(yī)般耐受性良好。
根據協議(yì)條款,Pyramid Biosciences将開(kāi)發和(hé)商業化GQ1010,啓德藥物(wù)将獲得2000萬美元的預付款和(hé)10億美元的額外(wài)裏程碑付款,GeneQuantum還将有資格獲得基于淨銷售額的特許權使用費(fèi)。
GQ1010通(tōng)過GeneQuantum在開(kāi)發差異化生物(wù)偶聯藥物(wù)(如(rú)抗HER2 ADC)方面,尖端技術(shù)展現了(le)在同類藥物(wù)中的最佳潛力。GQ1010采用獨特的位點特異性偶聯技術(shù),并結合了(le)一(yī)種新的鏈接(linker-payload),可(kě)提高ADC的穩定性、安全性和(hé)效力。臨床前數(shù)據表明(míng),與更先進的TROP2 ADCs相比,GQ1010具有更廣泛的治療餘量,這(zhè)可(kě)能(néng)轉化為(wèi)GQ1010的療效和(hé)安全性的改善。TROP2是一(yī)種細胞表面糖蛋白,在乳腺癌、肺癌、胰腺癌、卵巢癌和(hé)前列腺癌等多種腫瘤中高表達,并在腫瘤細胞增殖中發揮作(zuò)用。
2023年(nián)3月22日,Biohaven Ltd宣布與杭州高光(guāng)制藥有限公司達成在大中華區(qū)域以外(wài)的獨家開(kāi)發與許可(kě)協議(yì),引進高光(guāng)制藥研發的TLL-041。根據協議(yì),Biohaven将支付2000 萬美元首付款(現金(jīn)+股票)、9.5億美元裏程碑款及多層次、比例不等的銷售分成。Biohaven 将在2023 年(nián)啓動臨床Ⅰ期,雙方在全球協作(zuò)進行(xíng)臨床開(kāi)發。
TLL-041是全球首個具有通(tōng)過血腦屏障能(néng)力的高選擇性雙靶點 TYK2/JAK1抑制劑。TYK2 和(hé)JAK1是處理一(yī)系列促炎症細胞因子的STAT通(tōng)路調節劑;抑制這(zhè)些激酶可(kě)能(néng)在減少(shǎo)神經系統疾病的炎症方面發揮重要(yào)作(zuò)用,包括帕金(jīn)森病、阿爾茨海(hǎi)默病、肌萎縮性側索硬化症和(hé)多發性硬化症。TLL-041已經證明(míng)了(le)對JAK2、JAK3和(hé)其他(tā)激酶的高選擇性,與選擇性較低(dī)或無選擇性的JAK抑制劑相比,有可(kě)能(néng)提供更好的安全性。TLL-041的作(zuò)用機理在多個臨床前模型中得到證明(míng)。TLL-041由高光(guāng)制藥創始人(rén)梁從(cóng)新博士發明(míng),梁博士也是舒尼替尼、恩沙替尼、TLL-018等多個已上(shàng)市新藥、已進入上(shàng)市申報階段、臨床Ⅲ期階段新藥的發明(míng)人(rén)。
BHV-8000(TLL-041)具有通(tōng)過血腦屏障能(néng)力并對 TYK2/JAK1的雙重抑制作(zuò)用,為(wèi)治療腦部疾病提供了(le)獨特和(hé)極具吸引力的潛力。Biohaven将繼續推動 BHV-8000 進入臨床開(kāi)發,并發掘神經免疫調節的潛力,以治療急需新型治療方案的嚴重神經系統疾病。
2023年(nián)1月10日,緻力于創新藥研發的信諾維醫(yī)藥科技股份有限公司宣布與緻力于在腫瘤領域研發創新性療法的臨床階段生物(wù)醫(yī)藥公司AmMax Bio達成合作(zuò)。雙方就一(yī)款用于實體瘤治療的創新性ADC達成除大中華區(qū)外(wài)的全球研發和(hé)商業化的獨家轉讓權協議(yì)。該獨家轉讓權協議(yì)包含雙方協商好的授權條款(licensing terms),協議(yì)執行(xíng)後,信諾維将獲得最高達8.71億美元的支付款,包含首付款和(hé)開(kāi)發,注冊及銷售裏程碑。同時(shí)按照本協議(yì),雙方将協作(zuò)完成合作(zuò)項目的IND申請(qǐng)以及劑量遞增臨床研究的設計。
該ADC采用新一(yī)代的毒素-鏈接(linker-payload)和(hé)抗體, 并已經在多種臨床前動物(wù)模型中展現出優越的抗腫瘤活性,預期可(kě)用于多種實體瘤的治療。同時(shí),臨床前的療效和(hé)毒理研究表明(míng)該ADC具有更寬的治療窗口。目前已有數(shù)據表明(míng),該ADC的臨床療效和(hé)安全性特征對比同類ADC項目将會有大幅提高。
根據協議(yì)條款,君實生物(wù)将向瑞迪博士實驗室授予許可(kě),于巴西(xī)、墨西(xī)哥、哥倫比亞、阿根廷、秘魯、智利、巴拿(ná)馬、烏拉圭、印度及南非開(kāi)發及獨占地(dì)商業化特瑞普利單抗。瑞迪博士實驗室可(kě)選擇在獨占期內(nèi)将許可(kě)範圍擴大至涵蓋澳大利亞及新西(xī)蘭以及其他(tā)9個國(guó)家。
特瑞普利單抗注射液(拓益®)作(zuò)為(wèi)我國(guó)批準上(shàng)市的首個國(guó)産以PD-1為(wèi)靶點的單抗藥物(wù),獲得國(guó)家科技重大專項項目支持,并榮膺國(guó)家專利領域最高獎項“中國(guó)專利金(jīn)獎”。
特瑞普利單抗至今已在全球(包括中國(guó)、美國(guó)、東南亞及歐洲等地(dì))開(kāi)展了(le)覆蓋超過15個适應症的40多項由公司發起的臨床研究。正在進行(xíng)或已完成的關鍵注冊臨床研究在多個瘤種範圍內(nèi)評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
10:SHR2554(EZH2抑制劑)
授權方:恒瑞醫(yī)藥 引進方:Treeline Biosciences
2023年(nián)2月12日,恒瑞醫(yī)藥股份宣布與美國(guó)Treeline公司達成協議(yì),将具有自(zì)主知識産權的抗腫瘤藥品SHR2554(EZH2抑制劑)項目有償許可(kě)給Treeline公司。Treeline公司将獲得在除大中華區(qū)以外(wài)的全球範圍內(nèi)開(kāi)發、生産和(hé)商業化SHR2554的獨占權利。協議(yì)簽訂10天內(nèi),Treeline将向恒瑞支付1,100萬美元的首付款及6.95億美元的開(kāi)發、銷售裏程碑付款。同時(shí),從(cóng)SHR2554在許可(kě)區(qū)域啓動商業銷售開(kāi)始,Treeline将按照約定比例(10%-12.5%),根據實際年(nián)淨銷售額向恒瑞支付銷售提成。
SHR2554 為(wèi)恒瑞自(zì)主研發且具有知識産權的 EZH2(zeste 基因增強子同源物(wù)2)抑制劑。2018年(nián)5月,SHR2554獲批開(kāi)展治療複發/難治成熟淋巴細胞腫瘤的I期臨床研究。2023年(nián)1月,SHR2554被國(guó)家藥監局藥品審評中心納入突破性治療品種名單,用于複發或難治的外(wài)周T細胞淋巴瘤。截至目前,該産品已投入研發費(fèi)用約為(wèi)8,938萬元人(rén)民币。
與市場上(shàng)其他(tā)同類産品相比,Epizyme公司(已被Ipsen收購)的同類産品Tazverik(tazemetostat)已于2020年(nián)1月被美國(guó)食品藥品監督管理局(FDA)批準上(shàng)市,用于治療成人(rén)與16歲以上(shàng)青少(shǎo)年(nián)轉移性或局部晚期上(shàng)皮樣肉瘤(ES);同年(nián)6月,批準成人(rén)複發/難治性濾泡性淋巴瘤(r/rFL)适應症。其他(tā)同類産品還包括輝瑞公司的PF-06821497、第一(yī)三共制藥的valemetostat和(hé)Constellation(已被Morphosys收購)的CPI-0209。